Lurasidona - Lurasidone
 | |
 | |
| Datos clinicos | |
|---|---|
| Pronunciación | / lj ʊəˈr æ s ɪ d oʊ n / |
| Nombres comerciales | Latuda, otros |
| Otros nombres | SM-13496 |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a611016 |
| Datos de licencia | |
Categoría de embarazo |
|
| Vías de administración |
Oral |
| Clase de droga | Antipsicótico atípico |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | 9-19% (oral) |
| Enlace proteico | ~ 99% |
| Metabolismo | Hígado ( mediado por CYP3A4 ) |
| Vida media de eliminación | 18 a 40 horas |
| Excreción | Fecal (67 a 80%), renal (9 a 19%) |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Tarjeta de información ECHA |
100.225.187 |
| Datos químicos y físicos | |
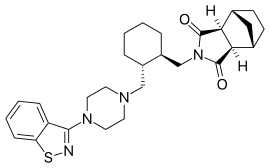
| Fórmula | C 28 H 36 N 4 O 2 S |
| Masa molar | 492,68 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| Rotacion especifica | [α] 20 D −59 ° |
| Punto de fusion | 176 a 178 ° C (349 a 352 ° F) |
| solubilidad en agua | 0,224 |
| |
| |
La lurasidona , vendida bajo el nombre comercial Latuda entre otros, es un medicamento antipsicótico que se usa para tratar la esquizofrenia y el trastorno bipolar . En bipolar se puede utilizar junto con un estabilizador del estado de ánimo como el litio o valproato . Se toma por vía oral.
Los efectos secundarios comunes incluyen somnolencia, trastornos del movimiento , náuseas y diarrea. Los efectos secundarios graves pueden incluir el trastorno del movimiento potencialmente permanente discinesia tardía , así como el síndrome neuroléptico maligno , un mayor riesgo de suicidio , angioedema y niveles altos de azúcar en sangre. En las personas mayores con psicosis como resultado de la demencia , puede aumentar el riesgo de muerte. El uso durante el embarazo no es de seguridad clara. No está claro cómo funciona, pero se cree que tiene efectos sobre la dopamina y la serotonina en el cerebro.
La lurasidona fue aprobada para uso médico en los Estados Unidos en 2010. En 2019 se aprobaron versiones genéricas en los Estados Unidos, pero no estarán disponibles hasta 2023. En 2018, fue el medicamento 245o más comúnmente recetado en los Estados Unidos, con más de 2 millones de recetas.
Usos médicos
La lurasidona se usa para el tratamiento de la esquizofrenia y el trastorno bipolar .
En Estados Unidos, la lurasidona está indicada para el tratamiento de:
- esquizofrenia en adultos y adolescentes (13 a 17 años)
- episodio depresivo asociado con trastorno bipolar I ( depresión bipolar ) en adultos y pacientes pediátricos (10 a 17 años) como monoterapia
- Episodio depresivo asociado con el trastorno bipolar I (depresión bipolar) en adultos como terapia adyuvante con litio o valproato.
En la Unión Europea, la lurasidona está indicada para el tratamiento de la esquizofrenia en adultos mayores de 18 años.
Una revisión de 2014 encontró que la lurasidona es similar en efectividad a otros antipsicóticos atípicos. Una revisión de 2013 de 15 medicamentos antipsicóticos en la esquizofrenia encontró que la lurasidona demostró una efectividad leve. Se considera que es tan eficaz como la iloperidona y de un 13 a un 15% menos eficaz que la ziprasidona , la clorpromazina y la asenapina .
En julio de 2013, la lurasidona recibió la aprobación para la depresión bipolar I. Se sabe que pocos antipsicóticos atípicos disponibles poseen eficacia antidepresiva en el trastorno bipolar (con las notables excepciones de quetiapina , olanzapina y posiblemente asenapina) como monoterapia, aunque se sabe que la mayoría de los antipsicóticos atípicos poseen una actividad antimaníaca significativa , que aún no se ha realizado. claramente demostrado para lurasidona.
En el período posterior a la aprobación temprana, se encontró retrospectivamente que los pacientes tratados con lurasidona con trastorno bipolar tenían perfiles clínicos, comorbilidades e historial de tratamiento previo más complejos en comparación con los pacientes que comenzaron con otros antipsicóticos atípicos. Los autores del estudio sugieren que esto puede deberse al "perfil clínico general de la lurasidona, el papel que los médicos perciben de la lurasidona en el arsenal terapéutico y la reciente introducción de la lurasidona en la práctica clínica durante el período de estudio".
La lurasidona no está aprobada por la Administración de Alimentos y Medicamentos (FDA) para el tratamiento de trastornos de conducta en adultos mayores con demencia.
Contraindicaciones
La lurasidona está contraindicada en personas que toman inhibidores potentes de la enzima hepática CYP3A4 ( ketoconazol , claritromicina , ritonavir , levodropropizina , etc.) o inductores ( carbamazepina , hierba de San Juan , fenitoína , rifampicina , etc.). No se ha estudiado y no se recomienda el uso de lurasidona en mujeres embarazadas; en estudios con animales, no se han encontrado riesgos. También se desconoce la excreción en la leche materna; No se recomienda la lurasidona para mujeres en período de lactancia. En los Estados Unidos no está indicado para su uso en niños.
Efectos secundarios
Los efectos secundarios son generalmente similares a otros antipsicóticos. El fármaco tiene un perfil de efectos secundarios relativamente bien tolerado , con baja propensión a cambios en el intervalo QTc , aumento de peso y efectos adversos relacionados con los lípidos . En un metanálisis de 2013 sobre la eficacia y tolerabilidad de 15 fármacos antipsicóticos, se encontró que producía el segundo menor aumento de peso (después del haloperidol ), la menor prolongación del intervalo QT, el cuarto efecto secundario más extrapiramidal (después del haloperidol , la zotepina y la clorpromazina ). y el sexto menor sedación (después de paliperidona , sertindol , amisulprida , iloperidona y aripiprazol ).
Al igual que con otros neurolépticos atípicos, la lurasidona debe usarse con precaución en los ancianos porque los pone en mayor riesgo de sufrir un accidente cerebrovascular o un ataque isquémico transitorio ; sin embargo, no es probable que estos riesgos sean mayores que los asociados con los antipsicóticos de otras clases. De manera similar, la lurasidona no debe usarse para tratar la psicosis relacionada con la demencia, ya que la evidencia ha demostrado un aumento de la mortalidad con el uso de antipsicóticos.
Se informa aumento de peso en hasta el 15 y el 16 por ciento de los usuarios.
Discontinuación
El Formulario Nacional Británico recomienda una retirada gradual al suspender los antipsicóticos para evitar el síndrome de abstinencia aguda o una recaída rápida. Los síntomas de abstinencia comúnmente incluyen náuseas, vómitos y pérdida del apetito. Otros síntomas pueden incluir inquietud, aumento de la sudoración y dificultad para dormir. Con menos frecuencia, puede haber una sensación de que el mundo da vueltas, entumecimiento o dolores musculares. Los síntomas generalmente se resuelven después de un corto período de tiempo.
Existe evidencia tentativa de que la interrupción de los antipsicóticos puede provocar psicosis. También puede resultar en la reaparición de la afección que se está tratando. Rara vez puede ocurrir discinesia tardía cuando se suspende el medicamento.
Interacciones
Las concentraciones plasmáticas sanguíneas pueden aumentar cuando se combinan con inhibidores de CYP3A4, lo que posiblemente produzca más efectos secundarios. Esto se ha verificado clínicamente para el ketoconazol , que aumenta la exposición a lurasidona en un factor de 9, y también se espera para otros inhibidores de 3A4 como el jugo de toronja . La coadministración de inductores de CYP3A4 como la rifampicina o la hierba de San Juan puede reducir los niveles plasmáticos de lurasidona y su metabolito activo y, en consecuencia, disminuir los efectos del fármaco. Para la rifampicina, la reducción fue seis veces mayor en un estudio.
Farmacología
Farmacodinamia
| Sitio | K yo (nM) | Acción | Especies | Árbitro |
|---|---|---|---|---|
| SERT | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| NETO | DAKOTA DEL NORTE | DAKOTA DEL NORTE | DAKOTA DEL NORTE | DAKOTA DEL NORTE |
| DAT | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| 5-HT 1A | 6,75 | Agonista parcial | Rata | |
| 5-HT 2A | 2.03 | Antagonista | Rata | |
| 5-HT 2B | DAKOTA DEL NORTE | DAKOTA DEL NORTE | DAKOTA DEL NORTE | DAKOTA DEL NORTE |
| 5-HT 2C | 415 | DAKOTA DEL NORTE | Cerdo | |
| 5-HT 3 | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| 5-HT 4 | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| 5-HT 7 | 0,495 | Antagonista | Humano | |
| α 1 | 47,9 | DAKOTA DEL NORTE | Rata | |
| α 2A | 40,7 | DAKOTA DEL NORTE | Humano | |
| α 2B | DAKOTA DEL NORTE | DAKOTA DEL NORTE | DAKOTA DEL NORTE | DAKOTA DEL NORTE |
| α 2C | 10,8 | Antagonista | Humano | |
| β 1 | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| β 2 | > 1000 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| D 1 | 262 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | |
| D 2 | 1,68 | Antagonista | Rata | |
| D 3 | 15,7 | Antagonista | DAKOTA DEL NORTE | DAKOTA DEL NORTE |
| D 4,4 | 30 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | DAKOTA DEL NORTE |
| D 5 | DAKOTA DEL NORTE | DAKOTA DEL NORTE | DAKOTA DEL NORTE | DAKOTA DEL NORTE |
| H 1 | > 1000 | DAKOTA DEL NORTE | conejillo de indias | |
| M 1 | > 1000 | DAKOTA DEL NORTE | Humano | |
| Los valores son K i (nM). Cuanto menor es el valor, más fuertemente se une el fármaco al sitio. | ||||
Lurasidone actúa como un antagonista de la dopamina D 2 y D 3 receptores , la serotonina 5-HT 2A y 5-HT 7 receptores , y la α 2C receptor adrenérgico , y como un agonista parcial de la serotonina 5-HT 1A receptor . Tiene solamente bajo y es probable clínicamente sin importancia afinidad para la serotonina 5-HT 2C receptor , que puede ser la base de su baja propensión a la estimulación del apetito y aumento de peso . El fármaco también tiene afinidad despreciable para la histamina H 1 receptor y los receptores muscarínicos de acetilcolina , y por lo tanto no tiene antihistamínico o anticolinérgicos efectos.
Farmacocinética


La lurasidona se toma por vía oral y tiene una tasa de absorción estimada del 9 al 19%. Los estudios han demostrado que cuando se toma lurasidona con alimentos, la absorción aumenta aproximadamente al doble. Las concentraciones máximas en plasma sanguíneo se alcanzan después de una a tres horas. Aproximadamente el 99% de la sustancia circulante se une a las proteínas plasmáticas .
La lurasidona se metaboliza principalmente en el hígado a través de la enzima CYP3A4, pero tiene una afinidad insignificante por otras enzimas del citocromo P450 . Es transportado por la glicoproteína P y ABCG2 y también inhibe estas proteínas transportadoras in vitro . También inhibe la proteína transportadora de solutos SLC22A1 , pero ningún otro transportador relevante.
Las principales vías de metabolismo son la N- desalquilación oxidativa entre los anillos de piperazina y ciclohexano, la hidroxilación del anillo norborano y la S-oxidación. : 59 Otras vías son la hidroxilación del anillo de ciclohexano y la escisión reductora del anillo de isotiazol seguida de S- metilación . Los dos metabolitos activos relevantes son los productos de hidroxilación del norborano denominados ID-14283 e ID-14326, alcanzando el primero concentraciones plasmáticas sanguíneas farmacológicamente relevantes. Los dos metabolitos inactivos principales son los productos de N-desalquilación (el ácido carboxílico ID-20219 y la piperazina ID-11614) y un derivado hidroxilado de norbornane de ID-20219 (ID-20220). De la lurasidona y sus metabolitos que circulan en la sangre, el fármaco nativo constituye el 11%, el principal metabolito activo el 4% y los ácidos carboxílicos inactivos el 24% y el 11%, respectivamente. Se han identificado en total varias docenas de metabolitos. : 59–61
La vida media biológica se da en 18 horas o de 20 a 40 horas en diferentes fuentes. El 80% o 67% de una dosis radiomarcada se recuperó de las heces y el 9% o 19% de la orina.
Historia
La lurasidona se fabricó en 2003.
La lurasidona es un análogo estructural de ziprasidona . La lurasidona muestra un perfil farmacológico muy cercano y se ha sintetizado de manera similar a la ziprasidona.
La lurasidona es químicamente similar a la perospirona (también un análogo químico de la ziprasidona), así como a la risperidona , paliperidona e iloperidona .
Cuenta con la aprobación de la Administración de Drogas y Alimentos de los EE. UU . (FDA) para el tratamiento de la esquizofrenia desde 2010 y para el tratamiento de episodios depresivos en adultos con trastorno bipolar I desde 2013.
sociedad y Cultura
Costo
En Canadá, a partir de 2014, la lurasidona es generalmente más cara que la risperidona y la quetiapina, pero menos cara que el aripiprazol .
En los EE. UU., Debido a que varias dosis tienen el mismo precio por tableta, se ha utilizado la división de píldoras para reducir los costos. En 2019 se aprobaron versiones genéricas en Estados Unidos; sin embargo, no estarán disponibles hasta 2023.
Nombres comerciales
En la India, este medicamento está disponible con las marcas Atlura, Lurace, Lurafic, Luramax, Lurasid, Lurastar, Latuda, Lurata y, además, como Alsiva, Emsidon, Lurakem, Luratrend, Tablura y Unison.
Aprobación regulatoria
La lurasidona fue aprobada en los Estados Unidos para el tratamiento de la esquizofrenia en octubre de 2010 y para el tratamiento de episodios depresivos asociados con el trastorno bipolar I en junio de 2013. Recibió la aprobación regulatoria en el Reino Unido en septiembre de 2014. En octubre de 2014, NHS Escocia aconsejó uso de lurasidona para adultos esquizofrénicos que no han visto mejoras con antipsicóticos anteriores debido a problemas que surgen del aumento de peso o cambios en las vías metabólicas al tomar otros medicamentos. El Comité de Medicamentos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos (EMA) emitió un dictamen positivo al respecto en enero de 2014, y fue aprobado para uso médico por la EMA en marzo de 2014. Fue lanzado en Canadá para el tratamiento de la esquizofrenia en septiembre de 2012, Health Canada dio su Resumen de la base de la decisión (SBD) como favorable el 15 de octubre de 2012. La Comisión Europea ha otorgado una autorización de comercialización para la lurasidona oral una vez al día para el tratamiento de la esquizofrenia en adultos. Está aprobado para su uso en la UE.
Las versiones genéricas de lurasidona se aprobaron para su uso en los Estados Unidos en enero de 2019.
Ver también
Referencias
enlaces externos
- "Lurasidona" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.
- "Comunicado de la FDA sobre la seguridad de los medicamentos: la FDA insta a la precaución sobre la retención de medicamentos para la adicción a los opioides de los pacientes que toman benzodiazepinas o depresores del SNC: el manejo cuidadoso de los medicamentos puede reducir los riesgos" . EE.UU. Administración de Drogas y Alimentos (FDA) . 7 de enero de 2021.

