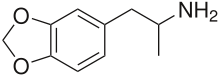
3,4-Metilendioxianfetamina - 3,4-Methylenedioxyamphetamine
 | |
 | |
| Datos clinicos | |
|---|---|
| Vías de administración |
Oral, sublingual, insuflación, intravenosa |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Metabolismo | Hepático ( CYP muy involucrado) |
| Excreción | Renal |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| CHEMBL | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA |
100.230.706 |
| Datos químicos y físicos | |
| Fórmula | C 10 H 13 N O 2 |
| Masa molar | 179,219 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
|
| |
La 3,4-metilendioxianfetamina (también conocida como MDA y sass ) es un empatógeno-entactógeno , psicoestimulante y droga psicodélica de la familia de las anfetaminas que se encuentra principalmente como droga recreativa . En términos de farmacología , la MDA actúa de manera más importante como un agente liberador de serotonina-norepinefrina-dopamina (SNDRA). En la mayoría de los países, la droga es una sustancia controlada y su posesión y venta son ilegales.
La MDA rara vez se busca como droga recreativa en comparación con otras drogas de la familia de las anfetaminas; sin embargo, sigue siendo un fármaco importante y ampliamente utilizado debido a que es un metabolito primario, producto de la N-desalquilación hepática, de MDMA (éxtasis). Además, es común encontrar MDA como adulterante de MDMA producido ilícitamente.
Usos
Médico
Actualmente, la MDA no tiene un uso médico aceptado.
Recreativo
Aunque es ilegal, la MDA se compra, vende y usa como una 'droga del amor' recreativa, debido a que mejora el estado de ánimo y la empatía . A veces se cita una dosis recreativa de MDA entre 100 y 160 mg.
Efectos adversos
La MDA produce efectos neurotóxicos serotoninérgicos, que se cree que se activan mediante el metabolismo inicial de la MDA. Además, MDA activa una respuesta de la neuroglia , aunque esta desaparece después de su uso.
Sobredosis
Los síntomas de toxicidad aguda pueden incluir agitación , sudoración , aumento de la presión arterial y frecuencia cardíaca , aumento dramático de la temperatura corporal , convulsiones y muerte . La muerte suele ser causada por efectos cardíacos y hemorragia cerebral posterior ( accidente cerebrovascular ).
Farmacología
Farmacodinamia
La MDA es un sustrato de los transportadores de serotonina , noradrenalina , dopamina y monoamina vesicular , así como un agonista de TAAR1 , y por estas razones actúa como inhibidor de la recaptación y agente liberador de serotonina , noradrenalina y dopamina (es decir, es un SNDRA ). También es un agonista de la serotonina 5-HT 2A , 5-HT 2B , y 5-HT 2C receptores y programas de afinidad para la α 2A - , α 2B - , y α 2C receptores adrenérgicos y de serotonina 5-HT 1A y Receptores 5-HT 7 .
El isómero óptico ( S ) de MDA es más potente que el isómero óptico ( R ) como psicoestimulante y posee una mayor afinidad por los tres transportadores de monoamina .
En términos de los efectos subjetivos y conductuales de la MDA, se cree que la liberación de serotonina es necesaria por sus efectos empatógeno-entactógeno, la liberación de dopamina y noradrenalina es responsable de sus efectos psicoestimulantes, la liberación de dopamina es necesaria por su euforia ( gratificante y adictiva ). efectos, y el agonismo directo del receptor de serotonina 5-HT 2A es causante de sus efectos psicodélicos.
Farmacocinética
Se ha informado que la duración del fármaco es de aproximadamente 6 a 8 horas.
Química
MDA es un derivado de fenetilamina y anfetamina metilendioxilada sustituida . En relación con otras fenetilaminas y anfetaminas, es el derivado de 3,4-metilendioxi, α-metilo de β-feniletilamina , el derivado de 3,4-metilendioxi de anfetamina y el derivado de N - desmetilo de MDMA.
Sinónimos
Además de la 3,4-metilendioxianfetamina , la MDA también se conoce por otros sinónimos químicos como los siguientes:
- α-Metil-3,4-metilendioxi-β-feniletilamina
- 1- (3,4-Metilendioxifenil) -2-propanamina
- 1- (1,3-benzodioxol-5-il) -2-propanamina
Síntesis
La MDA se sintetiza típicamente a partir de aceites esenciales como el safrol o el piperonal . Los enfoques comunes de estos precursores incluyen:
- Reacción del grupo funcional alqueno de safrol con un ácido mineral que contiene halógeno seguido de alquilación de amina .
- Oxidación de Wacker de safrol para producir 3,4-metilendioxifenilpropan-2-ona (MDP2P) seguida de aminación reductora o mediante reducción de su oxima .
- Reacción de Henry de piperonal con nitroetano seguida de reducción de compuestos nitro .
- La reacción de Darzens sobre heliotropina también fue realizada por J. Elks, et al. Esto da MDP2P , que luego se sometió a una reacción de Leuckart.
Detección en fluidos corporales
La MDA se puede cuantificar en sangre, plasma u orina para monitorear su uso, confirmar un diagnóstico de envenenamiento o ayudar en la investigación forense de un tráfico u otra infracción criminal o una muerte súbita. Algunos programas de detección de abuso de drogas se basan en el cabello, la saliva o el sudor como muestras. La mayoría de las pruebas de detección de inmunoensayo de anfetaminas comerciales tienen una reacción cruzada significativa con MDA y los principales metabolitos de MDMA, pero las técnicas cromatográficas pueden distinguir fácilmente y medir por separado cada una de estas sustancias. Las concentraciones de MDA en la sangre u orina de una persona que ha tomado solo MDMA son, en general, inferiores al 10% de las del fármaco original.
Derivados
MDA constituye parte de la estructura central del agonista del receptor β-adrenérgico protokylol .
Historia
La MDA fue sintetizada por primera vez por C. Mannich y W. Jacobsohn en 1910. Fue ingerida por primera vez en julio de 1930 por Gordon Alles, quien más tarde autorizó la droga a Smith, Kline & French . La MDA se utilizó por primera vez en pruebas con animales en 1939, y las pruebas en humanos comenzaron en 1941 en la exploración de posibles terapias para la enfermedad de Parkinson . De 1949 a 1957, más de 500 sujetos humanos recibieron MDA en una investigación de su uso potencial como antidepresivo y / o anoréxico por Smith, Kline & French . El Ejército de los Estados Unidos también experimentó con la droga, cuyo nombre en código EA-1298, mientras trabajaba para desarrollar una droga de verdad o un agente incapacitante. Harold Blauer murió en enero de 1953 después de que le inyectaran por vía intravenosa, sin su conocimiento o consentimiento, 450 mg de la droga como parte del Proyecto MKUltra . La MDA fue patentada como ataractica por Smith, Kline & French en 1960, y como anorexia bajo el nombre comercial "Amphedoxamine" en 1961. La MDA comenzó a aparecer en la escena de las drogas recreativas alrededor de 1963 a 1964. Entonces era barata y fácilmente disponible como producto químico de investigación de varias casas de suministros científicos. Varios investigadores, incluidos Claudio Naranjo y Richard Yensen , han explorado la MDA en el campo de la psicoterapia .
sociedad y Cultura
Nombre
Cuando la MDA se estaba desarrollando como posible fármaco farmacéutico, se le dio la denominación común internacional (DCI) de tenanfetamina .
Estatus legal
Australia
La MDA es una sustancia prohibida de la Lista 9 según los Estándares de Venenos . Una sustancia de la lista 9 se enumera como "Sustancias que pueden ser objeto de abuso o mal uso, cuya fabricación, posesión, venta o uso debería estar prohibido por la ley, excepto cuando sea necesario para la investigación médica o científica, o con fines analíticos, de enseñanza o de formación con aprobación de las Autoridades de Salud de la Commonwealth y / o del Estado o Territorio ".
Estados Unidos
La MDA es una sustancia controlada de la Lista I en los EE. UU.
Investigar
En 2010, se estudió la capacidad de la MDA para invocar experiencias místicas y alterar la visión en voluntarios sanos. El estudio concluyó que MDA es una "herramienta potencial para investigar experiencias místicas y percepción visual []".


