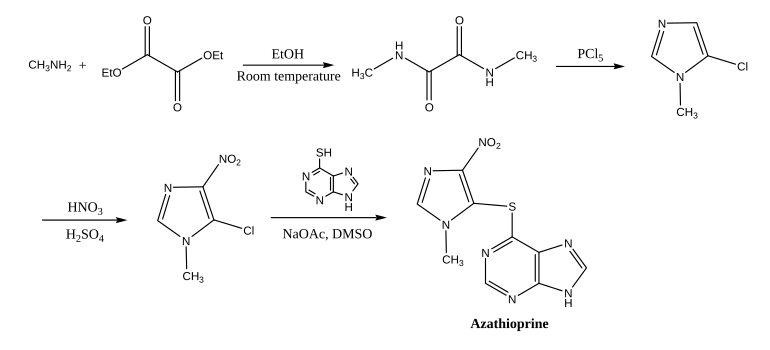
Azatioprina - Azathioprine
 | |
 | |
| Datos clinicos | |
|---|---|
| Pronunciación | / ˌ æ z ə theta aɪ ə ˌ p r i n / |
| Nombres comerciales | Azasan, Imuran y otros |
| AHFS / Drugs.com | Monografía |
| MedlinePlus | a682167 |
| Datos de licencia | |
Categoría de embarazo |
|
| Vías de administración |
Principalmente por vía oral (a veces inicialmente por vía intravenosa ) |
| Código ATC | |
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | 60 ± 31% |
| Enlace proteico | 20-30% |
| Metabolismo | Activado de forma no enzimática, desactivado principalmente por la xantina oxidasa |
| Vida media de eliminación | 26 a 80 minutos (azatioprina) 3 a 5 horas (fármaco más metabolitos) |
| Excreción | Riñón , 98% como metabolitos |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CHEBI | |
| CHEMBL | |
| Tablero CompTox ( EPA ) | |
| Tarjeta de información ECHA |
100.006.525 |
| Datos químicos y físicos | |
| Fórmula | C 9 H 7 N 7 O 2 S |
| Masa molar | 277,26 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| Punto de fusion | 238 a 245 ° C (460 a 473 ° F) |
| |
| |
| (verificar) | |
La azatioprina ( AZA ), que se vende bajo la marca Imuran , entre otros, es un medicamento inmunosupresor . Se utiliza en artritis reumatoide , granulomatosis con poliangeítis , enfermedad de Crohn , colitis ulcerosa y lupus eritematoso sistémico y en trasplantes de riñón para prevenir el rechazo . Se toma por vía oral o se inyecta en una vena .
Los efectos secundarios comunes incluyen supresión de la médula ósea y vómitos . La supresión de la médula ósea es especialmente común en personas con una deficiencia genética de la enzima tiopurina S-metiltransferasa . Otros factores de riesgo graves incluyen un mayor riesgo de ciertos cánceres . El uso durante el embarazo puede dañar al bebé. La azatioprina pertenece a la familia de medicamentos análogos de las purinas y antimetabolitos . Funciona a través de la 6-tioguanina para interrumpir la producción de ARN y ADN por parte de las células.
La azatioprina se fabricó por primera vez en 1957. Está en la Lista de medicamentos esenciales de la Organización Mundial de la Salud . En 2017, fue el medicamento 335 más comúnmente recetado en los Estados Unidos, con más de 800,000 recetas.
Usos médicos
La azatioprina se usa sola o en combinación con otra terapia inmunosupresora para prevenir el rechazo después del trasplante de órganos y para tratar una variedad de enfermedades autoinmunes , como artritis reumatoide , pénfigo , lupus eritematoso sistémico, enfermedad de Behçet y otras formas de vasculitis , hepatitis autoinmune , atópica. dermatitis , miastenia gravis , neuromielitis óptica (enfermedad de Devic), enfermedad pulmonar restrictiva y otras. También es una terapia importante y un agente ahorrador de esteroides para la enfermedad inflamatoria intestinal (como la enfermedad de Crohn y la colitis ulcerosa) y para la esclerosis múltiple .
En los Estados Unidos, está aprobado por la Administración de Drogas y Alimentos para su uso en el trasplante de riñón de donantes humanos y para la artritis reumatoide.
Trasplante
La azatioprina se usa para prevenir el rechazo de aloinjertos de riñón o hígado , generalmente junto con otras terapias, incluidos corticosteroides , otros inmunosupresores y radioterapia local . El protocolo de administración comienza en el momento del trasplante o dentro de los dos días siguientes.
Artritis reumatoide
Al ser un fármaco antirreumático modificador de la enfermedad (FARME), la azatioprina se ha utilizado para el tratamiento de los signos y síntomas de la artritis reumatoide en adultos . Los fármacos antiinflamatorios no esteroides y los corticosteroides se pueden combinar o continuar (si ya estaban en uso) con azatioprina, pero no se recomienda la combinación con otros FARME.
Enfermedad inflamatoria intestinal
La azatioprina se ha utilizado en el tratamiento de la enfermedad de Crohn activa crónica de moderada a grave, para mantener la remisión clínica (ausencia de actividad de la enfermedad) en pacientes dependientes de corticosteroides y para proporcionar beneficios en personas con enfermedad de Crohn fistulizante . El inicio de acción es lento y puede requerir varios meses para lograr la respuesta clínica.
El tratamiento con azatioprina se asocia con un mayor riesgo de linfoma , pero no está claro si esto se debe al fármaco oa una predisposición relacionada con la enfermedad de Crohn. Se utilizan dosis más bajas de azatioprina como terapia en niños con enfermedad de Crohn refractaria o dependiente de corticosteroides, sin causar muchos efectos secundarios. También se puede usar para prevenir brotes en personas con colitis ulcerosa .
Otros
En ocasiones, la azatioprina se usa en el lupus eritematoso sistémico, lo que requiere una dosis de mantenimiento de 15 mg o más de prednisona en aquellos que experimentan brotes recurrentes.
Se utiliza como terapia complementaria cuando la terapia con esteroides se administra por vía oral para el pénfigo y la miastenia grave, como un agente "ahorrador de esteroides". La azatioprina también se usa para mantener la remisión en personas que tienen granulomatosis con poliangeítis.
Puede ser muy eficaz en el eccema y la dermatitis atópica, aunque no se utiliza habitualmente. La Sociedad Nacional Británica de Eczema lo enumera como un tratamiento de tercera línea para casos severos a moderados de estas enfermedades de la piel.
Fue ampliamente utilizado para el tratamiento de la esclerosis múltiple hasta la primera mitad de la década de 1990. La preocupación por un mayor riesgo de malignidad ha llevado a un menor uso, sin embargo, todavía se usa en el tratamiento de mantenimiento para personas que recaen con frecuencia . Una revisión Cochrane de 2007 encontró que la azatioprina redujo el número de recaídas en el primer año de tratamiento y la progresión de la enfermedad en los primeros dos o tres años y no encontró un aumento en el cáncer, y señaló la necesidad de una comparación directa de azatioprina e interferón beta . conclusiones contradictorias sobre el cáncer y el potencial de riesgos a largo plazo.
Una terapia ampliamente utilizada para la fibrosis pulmonar idiopática fue la azatioprina en combinación con prednisona y N - acetilcisteína . Un estudio de 2012 mostró que los resultados fueron peores con esta combinación que con el placebo.
Efectos adversos
Las náuseas y los vómitos son efectos adversos frecuentes, especialmente al comienzo de un tratamiento. Tales casos se encuentran tomando azatioprina después de las comidas o con la administración intravenosa transitoria . Los efectos secundarios que probablemente sean reacciones de hipersensibilidad incluyen mareos, diarrea, fatiga y erupciones cutáneas . La pérdida de cabello se observa a menudo en pacientes trasplantados que reciben el fármaco, pero rara vez ocurre bajo otras indicaciones. Debido a que la azatioprina inhibe la médula ósea , los pacientes pueden desarrollar anemia y ser más susceptibles a las infecciones ; Se recomienda un control regular del hemograma durante el tratamiento. También puede ocurrir pancreatitis aguda , especialmente en pacientes con enfermedad de Crohn. El tratamiento se interrumpe hasta en un 30% de los pacientes debido a estos efectos, pero la monitorización terapéutica de los metabolitos biológicamente activos, es decir , los nucleótidos de tiopurina, puede ayudar a optimizar la eficacia y la seguridad. Clínicamente, la mayoría de los hospitales recurren a LC-MS en intercambio (cromatografía líquida - espectrometría de masas), pero el enfoque recientemente desarrollado de cromatografía basada en carbono grafítico poroso unida con espectrometría de masas parece superior con respecto a la atención del paciente en este sentido.
Según las reglas de la FDA, como muchos otros inmunosupresores, el uso de este medicamento excluye la elegibilidad para la donación de sangre .
Está catalogado por la Agencia Internacional para la Investigación del Cáncer como carcinógeno del grupo 1 (carcinógeno para los seres humanos).
Farmacogenética
La enzima tiopurina S-metiltransferasa (TPMT) es responsable de varios pasos de activación y desactivación en el mecanismo de acción de la azatioprina. El primer paso metabólico que sufre la azatioprina en el organismo es la conversión en 6-mercaptopurina (6-MP; ver Farmacocinética ), que es en sí mismo un profármaco inmunosupresor . La enzima TPMT es responsable, en parte, de la metilación de 6-MP en el metabolito inactivo 6-metilmercaptopurina; esta metilación evita que 6-MP se convierta más en metabolitos activos citotóxicos de nucleótidos de tioguanina (TGN). Ciertas variaciones genéticas dentro del gen TPMT pueden conducir a una actividad enzimática TPMT disminuida o ausente, y los individuos que son homocigotos o heterocigotos para estos tipos de variaciones genéticas pueden tener niveles aumentados de metabolitos TGN y un mayor riesgo de supresión severa de la médula ósea ( mielosupresión ) cuando recibir azatioprina. En muchas etnias, los polimorfismos de TPMT que dan como resultado una actividad de TPMT disminuida o ausente ocurren con una frecuencia de aproximadamente el 5%, lo que significa que aproximadamente el 0,25% de los pacientes son homocigotos para estas variantes. Sin embargo, un ensayo de actividad de TPMT en glóbulos rojos o una prueba genética de TPMT puede identificar pacientes con actividad de TPMT reducida, lo que permite el ajuste de la dosis de azatioprina o la evitación del fármaco por completo. La etiqueta del medicamento para azatioprina aprobada por la FDA recomienda realizar pruebas de actividad de TPMT para identificar a los pacientes en riesgo de mielotoxicidad . De hecho, la prueba de la actividad de TPMT es uno de los pocos ejemplos de farmacogenética que se traduce en atención clínica de rutina. Missense SNP en NUDT15 (p. Ej., Rs116855232, que induce R139C)) se ha identificado como un factor causal de leucopenia inducida por AZA a través de un estudio de asociación amplia del genoma (GWAS) en asiáticos orientales.
Cánceres
La azatioprina figura como carcinógeno humano en el 12 ° Informe sobre carcinógenos del Programa Nacional de Toxicología del Departamento de Salud y Servicios Humanos de EE. UU. , Afirmando que "se sabe que es un carcinógeno humano basado en pruebas suficientes de carcinogenicidad de estudios en humanos". Desde agosto de 2009, la FDA de EE. UU. Exige que se coloquen advertencias en los envases con respecto al aumento del riesgo de ciertos cánceres.
Los riesgos involucrados parecen estar relacionados tanto con la duración como con la dosis utilizada. Las personas que han sido tratadas previamente con un agente alquilante pueden tener un riesgo excesivo de cáncer si se tratan con azatioprina. Los estudios epidemiológicos de la Agencia Internacional para la Investigación del Cáncer han proporcionado evidencia "suficiente" de la carcinogenicidad de la azatioprina en humanos ( grupo 1 ), aunque se cuestiona la metodología de estudios anteriores y los posibles mecanismos subyacentes.
Las diversas enfermedades que requieren trasplante pueden aumentar por sí mismas los riesgos de linfoma no Hodgkin , carcinomas de células escamosas de la piel, carcinomas hepatobiliares y tumores mesenquimales a los que la azatioprina puede agregar riesgos adicionales. Los que reciben azatioprina para la artritis reumatoide pueden tener un riesgo menor que los que se someten a un trasplante.
Se han notificado casos de linfoma hepatoesplénico de células T , un tipo raro de linfoma , en pacientes tratados con azatioprina. La mayoría ocurrió en pacientes con enfermedad inflamatoria intestinal . Los adolescentes y los varones adultos jóvenes fueron la mayoría de los casos. Presentaron un curso de enfermedad muy agresivo y, con una excepción, murieron de linfoma. La FDA ha exigido cambios en el etiquetado para informar a los usuarios y médicos del problema.
Cánceres de piel
En los pacientes trasplantados, el cáncer de piel es de 50 a 250 veces más común que en la población general, y entre el 60 y el 90% de los pacientes se ven afectados 20 años después del trasplante. El uso de medicamentos inmunosupresores, incluida la azatioprina, en el trasplante de órganos se ha relacionado con un aumento de las tasas de cáncer de piel. La azatioprina provoca la acumulación de 6-tioguanina (6-TG) en el ADN de los pacientes, lo que podría desencadenar el cáncer cuando el paciente se expone posteriormente a la luz ultravioleta . Se encontró que los pacientes que tomaban azatioprina eran anormalmente sensibles a la luz UVA.
Sobredosis
Las grandes dosis únicas generalmente se toleran bien; un paciente que tomó 7,5 g de azatioprina (150 comprimidos) de una vez no mostró síntomas relevantes aparte de vómitos, recuento leve de glóbulos blancos y cambios marginales en los parámetros de función hepática. Los síntomas principales de una sobredosis a largo plazo son infecciones de origen poco claro, úlceras bucales y hemorragia espontánea, todos los cuales son consecuencia de su supresión de la médula ósea.
Interacciones
Otros análogos de la purina, como el alopurinol , inhiben la xantina oxidasa , la enzima que degrada la azatioprina, aumentando así la toxicidad de la azatioprina. Sin embargo, se ha demostrado que dosis bajas de alopurinol mejoran de manera segura la eficacia de la azatioprina, especialmente en quienes no responden a la enfermedad inflamatoria intestinal. Esto aún puede conducir a un menor recuento de linfocitos y mayores tasas de infección, por lo que la combinación requiere un control cuidadoso.
La azatioprina disminuye los efectos del anticoagulante warfarina y de los relajantes musculares no despolarizantes , pero aumenta el efecto de los relajantes musculares despolarizantes . También puede interferir con la niacina (vitamina B 3 ), lo que resulta en al menos un caso de pelagra y aplasia medular fatal.
Embarazo y lactancia
La azatioprina puede provocar defectos de nacimiento. Un estudio poblacional de 2003 en Dinamarca mostró que el uso de azatioprina y mercaptopurina relacionada resultó en una incidencia siete veces mayor de anomalías fetales, así como un aumento de 20 veces en el aborto espontáneo . También se han informado defectos de nacimiento en un niño cuyo padre estaba tomando azatioprina. Aunque no se han realizado estudios adecuados y bien controlados en humanos, cuando se administró a animales en dosis equivalentes a las dosis humanas, se observó teratogénesis. Las pacientes trasplantadas que ya están tomando este medicamento no deben interrumpir el tratamiento al quedar embarazadas. Esto contrasta con los fármacos de desarrollo posterior tacrolimus y micofenolato, que están contraindicados durante el embarazo.
Tradicionalmente, como para todos los medicamentos citotóxicos , el fabricante aconseja no amamantar mientras se toma azatioprina, pero la "categoría de riesgo de lactancia" informada por Thomas Hale en su libro Medications and Mothers 'Milk enumera la azatioprina como "L3", denominada "moderadamente segura".
Farmacología
Farmacocinética
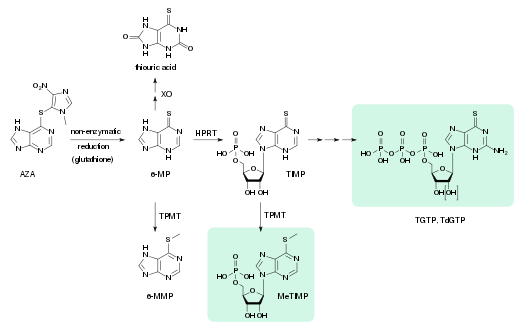
- XO: xantina oxidasa
- 6-MP: 6- mercaptopurina
- TPMT: tiopurina metiltransferasa
- 6-MMP: 6-metilmercaptopurina
- HPRT: hipoxantina-guanina fosforribosiltransferasa
- TIMP: monofosfato de tioinosina, ácido tioinosínico
- MeTIMP: monofosfato de metil-tioinosina
- TGTP: trifosfato de tio guanosina
- TdGTP: trifosfato de tiodesoxiguanosina
La azatioprina se absorbe en el intestino hasta aproximadamente un 88%. La biodisponibilidad varía mucho entre pacientes individuales, entre el 30 y el 90%, porque el fármaco se inactiva parcialmente en el hígado. Las concentraciones plasmáticas más altas, contando no sólo el fármaco en sí, sino también sus metabolitos, se alcanzan después de 1 a 2 horas, y la semivida plasmática media es de 26 a 80 minutos para la azatioprina y de 3 a 5 horas para el fármaco más metabolitos. Entre el 20 y el 30% se unen a las proteínas plasmáticas mientras circulan en el torrente sanguíneo.
La azatioprina es un profármaco , una sustancia que no es un fármaco activo en sí mismo, pero que se activa en el cuerpo. Esto sucede en varios pasos; al principio, se convierte lenta y casi por completo en 6-mercaptopurina (6-MP) mediante la escisión reductora del tioéter (- S -). Esto está mediado por el glutatión y compuestos similares en la pared intestinal, el hígado y los glóbulos rojos, sin la ayuda de enzimas. El 6-MP se metaboliza de forma análoga a las purinas naturales, dando trifosfato de tio guanosina (TGTP) y trifosfato de tio desoxiguanosina (TdGTP) a través del monofosfato de tioinosina (TIMP) y varios intermedios adicionales. En un segundo camino, el átomo de azufre de 6-MP y TIMP está metilado . Los productos finales del metabolismo de la azatioprina son el ácido tiurico (38%) y varias purinas metiladas e hidroxiladas , que se excretan por la orina.
Mecanismo de acción
La azatioprina inhibe la síntesis de purinas . Se necesitan purinas para producir ADN y ARN. Al inhibir la síntesis de purinas, se produce menos ADN y ARN para la síntesis de glóbulos blancos , lo que provoca inmunosupresión.
La azatioprina se convierte dentro de los tejidos en 6-MP, parte de la cual se convierte, a su vez, en 6-tioguanina mediante la adición de un grupo amino. Tanto la 6-MP como la 6-tioguanina se conjugan con ribosa y luego se fosforilan para formar los nucleótidos ácido tioinosínico y ácido tioguanílico, respectivamente. Estos nucleótidos se disfrazan, respectivamente, como ácido inosínico y ácido guanílico ; el primero es el punto de partida para la biosíntesis de nucleótidos de purina, mientras que el segundo es uno de los componentes básicos del ADN y el ARN.
- Los nucleótidos se incorporan al ADN recién sintetizado (pero no funcional), deteniendo la replicación .
- Los nucleótidos actúan para inhibir la glutamina- fosforribosil pirofosfato amidotransferasa (GPAT), una de las enzimas implicadas en la biosíntesis de purinas , uno de los primeros pasos en la síntesis de ADN y ARN. Logran la inhibición de GPAT a través de una forma de retroalimentación negativa llamada inhibición del producto . Dado que las células que se replican activamente (tales como las células cancerosas y las células T y las células B del sistema inmune ) son más activos en la síntesis de purina, haciendo nuevo ADN, estas células son las más fuertemente afectados.
- Una parte de los nucleótidos se fosforila adicionalmente a las formas trifosfato. Estos se unen a la proteína Rac1 de unión a GTP , bloqueando la síntesis de la proteína Bcl-xL , enviando así células T activadas y células mononucleares a la apoptosis (muerte celular programada). Se observa un aumento de la apoptosis de las células mononucleares en pacientes con enfermedad inflamatoria intestinal tratados con azatioprina.
Química
La azatioprina es una tiopurina unida a un segundo heterociclo (un derivado de imidazol ) a través de un tioéter . Es un sólido de color amarillo pálido con un sabor ligeramente amargo y un punto de fusión de 238–245 ° C. Es prácticamente insoluble en agua y solo ligeramente soluble en disolventes lipofílicos como cloroformo, etanol y éter dietílico. Se disuelve en soluciones acuosas alcalinas, donde se hidroliza a 6-mercaptopurina.
La azatioprina se sintetiza a partir de 5-cloro-1-metil-4-nitro- 1H -imidazol y 6-mercaptopurina en dimetilsulfóxido . La síntesis del primero comienza con una amida a partir de metilamina y oxalato de dietilo , que luego se cicla y clora con pentacloruro de fósforo ; el grupo nitro se introduce con ácido nítrico y sulfúrico .
Historia
La azatioprina fue sintetizada por George Herbert Hitchings y Gertrude Elion en 1957 (llamada BW 57-322) para producir 6-MP en una forma metabólicamente activa, pero enmascarada, y al principio se utilizó como fármaco de quimioterapia .
Robert Schwartz investigó el efecto del 6-MP sobre la respuesta inmune en 1958 y descubrió que suprime profundamente la formación de anticuerpos cuando se administra a conejos junto con antígenos . Siguiendo el trabajo realizado por Sir Peter Medawar y Gertrude Elion para descubrir la base inmunológica del rechazo de tejidos y órganos trasplantados, y las investigaciones de Schwartz sobre el 6-MP, Sir Roy Calne , el pionero británico en trasplantes, presentó el 6-MP como inmunosupresor experimental. para trasplantes de riñón y corazón . Cuando Calne le pidió a Elion que investigara compuestos relacionados, ella sugirió azatioprina, que posteriormente Calne descubrió que era superior (como eficaz y menos tóxica para la médula ósea).
El 5 de abril de 1962, con regímenes que consistían en azatioprina y prednisona, el trasplante de riñones a receptores no emparentados (alotrasplante) tuvo éxito por primera vez. Durante muchos años, este tipo de terapia dual con azatioprina y glucocorticoides fue el régimen antirrechazo estándar, hasta que la ciclosporina se introdujo en la práctica clínica (también por Calne) en 1978.
La ciclosporina ahora ha reemplazado parte del uso de azatioprina debido a un mayor tiempo de supervivencia, especialmente en los trasplantes relacionados con el corazón. Además, a pesar de ser considerablemente más caro, el micofenolato de mofetilo también se usa cada vez más en lugar de la azatioprina en el trasplante de órganos, ya que se asocia con una menor supresión de la médula ósea, menos infecciones oportunistas y una menor incidencia de rechazo agudo.
Referencias
Otras lecturas
- Dean L (2012). "Terapia de azatioprina y genotipo TPMT" . En Pratt VM, McLeod HL, Rubinstein WS, et al. (eds.). Resúmenes de genética médica . Centro Nacional de Información Biotecnológica (NCBI). PMID 28520349 . ID de estantería: NBK100661.
enlaces externos
- "Azatioprina" . Portal de información sobre medicamentos . Biblioteca Nacional de Medicina de EE. UU.