Hidroquinona - Hydroquinone

|
|
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
Benceno-1,4-diol |
|
| Otros nombres
Hidroquinona
Idroquinona Quinol 1,4-Dihidroxibenceno 1,4-Hidroxibenceno |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 605970 | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.004.199 |
| Número CE | |
| 2742 | |
| KEGG | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| un numero | 3077, 2662 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 6 H 6 O 2 | |
| Masa molar | 110,112 g · mol −1 |
| Apariencia | Blanco sólido |
| Densidad | 1,3 g cm −3 , sólido |
| Punto de fusion | 172 ° C (342 ° F; 445 K) |
| Punto de ebullición | 287 ° C (549 ° F; 560 K) |
| 5,9 g / 100 ml (15 ° C) | |
| Presión de vapor | 10 −5 mmHg (20 ° C) |
| Acidez (p K a ) | 9,9 |
| −64,63 × 10 −6 cm 3 / mol | |
| Estructura | |
| 1,4 ± 0,1 D | |
| Farmacología | |
| D11AX11 ( OMS ) | |
| Riesgos | |
| Nocivo ( Xn ) Carc. Gato. 3 Muta. Gato. 3 Peligroso para el medio ambiente ( N ) |
|
| Frases R (desactualizadas) | R22 R40 R41 R43 R50 R68 |
| Frases S (desactualizadas) | (S2) S26 S36 / 37/39 S61 |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | 165 ° C (329 ° F; 438 K) |
| Dosis o concentración letal (LD, LC): | |
|
LD 50 ( dosis media )
|
490 mg / kg (mamífero, oral) 245 mg / kg (ratón, oral) 200 mg / kg (conejo, oral) 320 mg / kg (rata, oral) 550 mg / kg (conejillo de indias, oral) 200 mg / kg (perro, oral) 70 mg / kg (gato, oral) |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
|
PEL (permitido)
|
TWA 2 mg / m 3 |
|
REL (recomendado)
|
C 2 mg / m 3 [15 minutos] |
|
IDLH (peligro inmediato)
|
50 mg / m 3 |
| Compuestos relacionados | |
|
Bencenodioles relacionados
|
Pyrocatechol Resorcinol |
|
Compuestos relacionados
|
1,4-benzoquinona |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
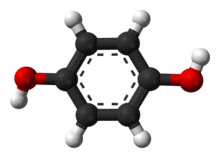
La hidroquinona , también conocida como benceno-1,4-diol o quinol , es un compuesto orgánico aromático que es un tipo de fenol , un derivado del benceno , que tiene la fórmula química C 6 H 4 (OH) 2 . Tiene dos grupos hidroxilo unidos a un anillo de benceno en posición para . Es un sólido granular blanco . Los derivados sustituidos de este compuesto original también se denominan hidroquinonas. El nombre "hidroquinona" fue acuñado por Friedrich Wöhler en 1843.
Producción
La hidroquinona se produce industrialmente de dos formas principales.
- La ruta más utilizada es similar al proceso de cumeno en el mecanismo de reacción e implica la dialquilación de benceno con propeno para dar 1,4-diisopropilbenceno. Este compuesto reacciona con el aire para producir el bis (hidroperóxido), que es estructuralmente similar al hidroperóxido de cumeno y se reordena en ácido para dar acetona e hidroquinona.
- Una segunda ruta implica la hidroxilación de fenol sobre un catalizador. La conversión usa peróxido de hidrógeno y produce una mezcla de hidroquinona y catecol (benceno-1,2-diol):
- C 6 H 5 OH + H 2 O 2 → C 6 H 4 (OH) 2 + H 2 O
Otros métodos menos comunes incluyen:
- Se ha propuesto una síntesis potencialmente significativa de hidroquinona a partir de acetileno y pentacarbonilo de hierro. El pentacarbonilo de hierro sirve como catalizador , más que como reactivo , en presencia de gas monóxido de carbono libre . El rodio o el rutenio pueden sustituir al hierro como catalizador con rendimientos químicos favorables, pero normalmente no se usan debido a su costo de recuperación de la mezcla de reacción.
- La hidroquinona y sus derivados también se pueden preparar por oxidación de varios fenoles. Los ejemplos incluyen la oxidación de persulfato de Elbs y la oxidación de Dakin :
- La hidroquinona fue obtenida por primera vez en 1820 por los químicos franceses Pelletier y Caventou mediante la destilación en seco de ácido quínico .
Reacciones
La reactividad de los grupos hidroxilo de la hidroquinona se asemeja a la de otros fenoles , siendo débilmente ácidos. La base conjugada resultante se somete a una fácil O- alquilación para dar mono y diéteres . De manera similar, la hidroquinona es muy susceptible a la sustitución del anillo por reacciones de Friedel-Crafts como la alquilación. Esta reacción se aprovecha en el camino de los antioxidantes populares como el 2- terc -butil-4-metoxifenol ( BHA ). La quinizarina colorante útil se produce por diacilación de hidroquinona con anhídrido ftálico .
Redox
La hidroquinona se oxida en condiciones suaves para dar benzoquinona . Este proceso se puede revertir. Algunos derivados de hidroquinona de origen natural presentan este tipo de reactividad, siendo un ejemplo coenzima Q . Industrialmente, esta reacción se explota tanto con la propia hidroquinona como con sus derivados en los que un OH ha sido reemplazado por una amina.
Cuando la hidroquinona incolora y la benzoquinona, un sólido amarillo brillante, se cocristalizan en una proporción de 1: 1, un complejo de transferencia de carga cristalino de color verde oscuro ( punto de fusión 171 ° C) llamado quinhidrona (C 6 H 6 O 2 · C 6 H 4 O 2 ) se forma. Este complejo se disuelve en agua caliente, donde las dos moléculas se disocian en solución.
Aminación
Una reacción importante es la conversión de hidroquinona en derivados de mono y diamina. El metilaminofenol , utilizado en fotografía, se produce de esta manera:
- C 6 H 4 (OH) 2 + CH 3 NH 2 → HOC 6 H 4 NHCH 3 + H 2 O
De manera similar, las diaminas, útiles en la industria del caucho como agentes antiozona, se producen de manera similar a partir de la anilina :
- C 6 H 4 (OH) 2 + 2 C 6 H 5 NH 2 → C 6 H 4 (N (H) C 6 H 5 ) 2 + 2 H 2 O
Usos
La hidroquinona tiene una variedad de usos asociados principalmente con su acción como agente reductor que es soluble en agua. Es un componente importante en la mayoría de los reveladores fotográficos en blanco y negro para películas y papel donde, con el compuesto metol , reduce los haluros de plata a plata elemental .
Hay varios otros usos asociados con su poder reductor . Como inhibidor de la polimerización , aprovechando sus propiedades antioxidantes , la hidroquinona previene la polimerización de ácido acrílico , metacrilato de metilo , cianoacrilato y otros monómeros que son susceptibles de polimerización iniciada por radicales . Al actuar como un eliminador de radicales libres, la hidroquinona sirve para prolongar la vida útil de las resinas sensibles a la luz como los polímeros precerámicos .
La hidroquinona puede perder un catión de hidrógeno de ambos grupos hidroxilo para formar un ion difenolato. La sal difenolato de sodio de hidroquinona se usa como una unidad de comonómero alterno en la producción del polímero PEEK .
Despigmentación de la piel
La hidroquinona se usa como aplicación tópica en el blanqueamiento de la piel para reducir el color de la piel. No tiene la misma predisposición a causar dermatitis que el metol . Este es un ingrediente solo con receta en algunos países, incluidos los estados miembros de la Unión Europea bajo las Directivas 76/768 / EEC: 1976.
En 2006, la Administración de Drogas y Alimentos de los Estados Unidos revocó su aprobación previa de hidroquinona y propuso la prohibición de todas las preparaciones de venta libre . La FDA declaró que no se puede descartar la hidroquinona como carcinógeno potencial . Se llegó a esta conclusión basándose en el grado de absorción en humanos y la incidencia de neoplasias en ratas en varios estudios donde se encontró que las ratas adultas tenían mayores tasas de tumores, incluidas hiperplasias de células foliculares tiroideas , anisocariosis (variación en el tamaño de los núcleos), células mononucleares leucemia, adenomas hepatocelulares y adenomas de células del túbulo renal . La Campaña para Cosméticos Seguros también ha puesto de relieve preocupaciones.
Numerosos estudios han revelado que la hidroquinona, si se toma por vía oral, puede causar ocronosis exógena , una enfermedad desfigurante en la que se depositan pigmentos azul-negros sobre la piel; sin embargo, las preparaciones para la piel que contienen el ingrediente se administran por vía tópica. La FDA había clasificado la hidroquinona en 1982 como un producto seguro, generalmente reconocido como seguro y eficaz (GRASE); sin embargo, se sugirieron estudios adicionales en el marco del Programa Nacional de Toxicología (NTP) para determinar si existe un riesgo para los seres humanos por el uso de hidroquinona. La evaluación del NTP mostró alguna evidencia de efectos cancerígenos y genotóxicos a largo plazo
Si bien el uso de hidroquinona como agente aclarador puede ser efectivo con un uso adecuado, también puede causar sensibilidad en la piel. El uso de un protector solar diario con un alto índice de PPD (oscurecimiento persistente del pigmento) reduce el riesgo de daños mayores. La hidroquinona a veces se combina con alfa-hidroxiácidos que exfolian la piel para acelerar el proceso de aclarado. En los Estados Unidos, los tratamientos tópicos suelen contener hasta un 2% de hidroquinona. De lo contrario, deben prescribirse concentraciones más altas (hasta 4%) y usarse con precaución.
Si bien la hidroquinona sigue siendo ampliamente prescrita para el tratamiento de la hiperpigmentación , las agencias reguladoras de la UE, Japón y EE. UU. Plantean preguntas sobre su perfil de seguridad que fomentan la búsqueda de otros agentes con eficacia comparable. Varios de estos agentes ya están disponibles o en investigación, incluidos ácido azelaico , ácido kójico , retinoides, cisteamina, esteroides tópicos, ácido glicólico y otras sustancias. Se ha demostrado que uno de estos, el 4-butilresorcinol , es más eficaz en el tratamiento de los trastornos de la piel relacionados con la melanina por un amplio margen, así como lo suficientemente seguro como para estar disponible sin receta.
Sucesos naturales
Las hidroquinonas son uno de los dos reactivos principales en las glándulas defensivas de los escarabajos bombarderos , junto con el peróxido de hidrógeno (y quizás otros compuestos, dependiendo de la especie), que se acumulan en un depósito. El depósito se abre a través de una válvula controlada por los músculos hacia una cámara de reacción de paredes gruesas. Esta cámara está revestida de células que secretan catalasas y peroxidasas . Cuando el contenido del depósito se fuerza a la cámara de reacción, las catalasas y peroxidasas descomponen rápidamente el peróxido de hidrógeno y catalizan la oxidación de las hidroquinonas en p -quinonas . Estas reacciones liberan oxígeno libre y generan suficiente calor para llevar la mezcla al punto de ebullición y vaporizar alrededor de una quinta parte, produciendo un rocío caliente desde el abdomen del escarabajo .
Los derivados de farnesil hidroquinona son los principales irritantes que exuda el arbusto del caniche , que puede causar dermatitis de contacto grave en humanos.
Se cree que la hidroquinona es la toxina activa de los hongos Agaricus hondensis .
Se ha demostrado que la hidroquinona es uno de los componentes químicos del propóleo producto natural .
También es uno de los compuestos químicos que se encuentran en el castóreo . Este compuesto se obtiene del castor sacos de ricino 's.
En la gayuba ( Arctostaphylos uva-ursi ), la arbutina se convierte en hidroquinona.

