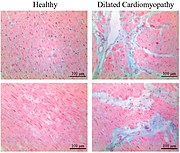
Diagnóstico de infarto de miocardio - Myocardial infarction diagnosis
| Diagnóstico de infarto de miocardio | |
|---|---|
| Objetivo | diagnosticar un infarto de miocardio mediante un examen físico y un electrocardiograma (más un análisis de sangre) |
Se crea un diagnóstico de infarto de miocardio integrando el historial de la enfermedad presente y el examen físico con los hallazgos del electrocardiograma y los marcadores cardíacos ( análisis de sangre para el daño de las células del músculo cardíaco ). Un angiograma coronario permite la visualización de estrechamientos u obstrucciones en los vasos cardíacos, y las medidas terapéuticas pueden seguir de inmediato. En la autopsia , un patólogo puede diagnosticar un infarto de miocardio basándose en los hallazgos anatomopatológicos .
Una radiografía de tórax y análisis de sangre de rutina pueden indicar complicaciones o causas precipitantes y, a menudo, se realizan al llegar al departamento de emergencias . Las nuevas anomalías regionales del movimiento de la pared en un ecocardiograma también sugieren un infarto de miocardio. En casos dudosos, el cardiólogo de guardia puede realizar la ecografía. En pacientes estables cuyos síntomas se han resuelto en el momento de la evaluación, se puede utilizar tecnecio (99mTc) sestamibi (es decir, una "exploración MIBI"), cloruro de talio-201 o cloruro de rubidio-82 en medicina nuclear para visualizar áreas de flujo sanguíneo reducido en junto con el estrés fisiológico o farmacológico. El talio también se puede utilizar para determinar la viabilidad del tejido, distinguiendo si el miocardio no funcional está realmente muerto o simplemente en estado de hibernación o aturdido.
Criterios de diagnóstico
De acuerdo con los criterios de la OMS revisados en 2000, un aumento de la troponina cardíaca acompañado de síntomas típicos, ondas Q patológicas, elevación o depresión del ST o intervención coronaria son diagnósticos de IM.
Los criterios previos de la OMS formulados en 1979 pusieron menos énfasis en los biomarcadores cardíacos; según estos, se diagnostica un infarto de miocardio a un paciente si se cumplen dos (probables) o tres (definitivos) de los siguientes criterios:
- Historia clínica de dolor torácico de tipo isquémico que dura más de 20 minutos
- Cambios en los trazados de ECG en serie
- Aumento y disminución de los biomarcadores cardíacos séricos como la creatina quinasa -fracción MB y la troponina
Examen físico
El aspecto general de los pacientes puede variar según los síntomas experimentados; el paciente puede sentirse cómodo o inquieto y con una angustia severa con un aumento de la frecuencia respiratoria . Una piel fría y pálida es común y apunta a vasoconstricción . Algunos pacientes tienen febrícula (38 a 39 ° C). La presión arterial puede estar elevada o disminuida y el pulso puede volverse irregular .
Si se produce insuficiencia cardíaca, en la inspección se puede encontrar presión venosa yugular elevada y reflujo hepatoyugular , o hinchazón de las piernas debido a edema periférico . En raras ocasiones, en el examen precordial se puede sentir una protuberancia cardíaca con un ritmo diferente al del pulso . Diversas anomalías se pueden encontrar en la auscultación , como tercera y cuarta sonido del corazón , soplos sistólicos , desdoblamiento paradójico del segundo sonido de corazón, un pericárdico roce y estertores sobre el pulmón.
Electrocardiograma

El objetivo principal del electrocardiograma es detectar isquemia o lesión coronaria aguda en poblaciones amplias y sintomáticas del servicio de urgencias . Se puede utilizar un ECG en serie para seguir cambios rápidos en el tiempo. El ECG estándar de 12 derivaciones no examina directamente el ventrículo derecho y es relativamente deficiente para examinar las paredes posterior basal y lateral del ventrículo izquierdo . En particular, es probable que el infarto agudo de miocardio en la distribución de la arteria circunfleja produzca un ECG no diagnóstico. El uso de derivaciones de ECG adicionales como las derivaciones del lado derecho V3R y V4R y las derivaciones posteriores V7, V8 y V9 puede mejorar la sensibilidad para el infarto de miocardio posterior y ventricular derecho.
El ECG de 12 derivaciones se utiliza para clasificar a los pacientes en uno de tres grupos:
- aquellos con elevación del segmento ST o nuevo bloqueo de rama (sospechosos de lesión aguda y posible candidato para terapia de reperfusión aguda con trombolíticos o ICP primaria ),
- aquellos con depresión del segmento ST o inversión de la onda T (sospechosos de isquemia), y
- aquellos con un ECG normal o no diagnóstico.
Un ECG normal no descarta un infarto agudo de miocardio. Los errores de interpretación son relativamente comunes y el hecho de no identificar las características de alto riesgo tiene un efecto negativo en la calidad de la atención al paciente.
Se debe determinar si una persona tiene un alto riesgo de infarto de miocardio antes de realizar pruebas de imagen para hacer un diagnóstico. Las personas que tienen un ECG normal y que pueden hacer ejercicio, por ejemplo, no merecen la obtención de imágenes de rutina. Las pruebas de imagen, como las imágenes de perfusión miocárdica con radionúclidos de estrés o la ecocardiografía de estrés, pueden confirmar un diagnóstico cuando los antecedentes, el examen físico, el ECG y los biomarcadores cardíacos de una persona sugieren la probabilidad de un problema.
Marcadores cardiacos
Los marcadores cardíacos o enzimas cardíacas son proteínas que se escapan de las células miocárdicas lesionadas a través de sus membranas celulares dañadas hacia el torrente sanguíneo. Hasta la década de 1980, las enzimas SGOT y LDH se utilizaron para evaluar la lesión cardíaca. Ahora, los marcadores más utilizados en la detección de IM son el subtipo MB de la enzima creatina quinasa y las troponinas cardíacas T e I, ya que son más específicas para la lesión miocárdica. Las troponinas cardíacas T e I, que se liberan entre 4 y 6 horas después de un ataque de MI y permanecen elevadas hasta por 2 semanas, tienen una especificidad tisular casi completa y ahora son los marcadores preferidos para evaluar el daño miocárdico. La proteína de unión a ácidos grasos de tipo corazón es otro marcador que se utiliza en algunos kits de prueba caseros. Las troponinas elevadas en el contexto de dolor torácico pueden predecir con precisión una alta probabilidad de infarto de miocardio en un futuro próximo. Se están investigando nuevos marcadores como la isoenzima BB de la glucógeno fosforilasa .
El diagnóstico de infarto de miocardio requiere dos de tres componentes (antecedentes, ECG y enzimas). Cuando se produce un daño en el corazón, los niveles de marcadores cardíacos aumentan con el tiempo, por lo que se realizan análisis de sangre durante un período de 24 horas. Debido a que estos niveles de enzimas no se elevan inmediatamente después de un ataque cardíaco, los pacientes que presentan dolor en el pecho generalmente se tratan con la suposición de que ha ocurrido un infarto de miocardio y luego se evalúan para un diagnóstico más preciso.
Angiografía

En casos difíciles o en situaciones donde la intervención para restaurar el flujo sanguíneo es apropiada, se puede realizar una angiografía coronaria . Se inserta un catéter en una arteria (generalmente la arteria radial o femoral ) y se empuja hacia los vasos que irrigan el corazón. Se administra un tinte radiopaco a través del catéter y se realiza una secuencia de radiografías (fluoroscopia). Se pueden identificar las arterias obstruidas o estrechas y aplicar una angioplastia como medida terapéutica (ver más abajo). La angioplastia requiere una gran habilidad, especialmente en situaciones de emergencia. Lo realiza un médico capacitado en cardiología intervencionista .
Histopatología
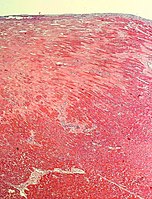
El examen histopatológico del corazón puede revelar un infarto en la autopsia . El examen macroscópico puede revelar signos de infarto de miocardio.
Bajo el microscopio, el infarto de miocardio se presenta como un área circunscrita de necrosis coagulativa isquémica (muerte celular). En el examen macroscópico, el infarto no es identificable dentro de las primeras 12 horas.
Aunque los cambios más tempranos se pueden discernir usando microscopía electrónica , uno de los primeros cambios bajo un microscopio normal son las llamadas fibras onduladas . Posteriormente, el citoplasma del miocito se vuelve más eosinofílico (rosa) y las células pierden sus estrías transversales, con cambios típicos y eventualmente pérdida del núcleo celular . El intersticio en el margen del área infartada se infiltra inicialmente con neutrófilos , luego con linfocitos y macrófagos , que fagocitan ("comen") los restos de miocitos. El área necrótica está rodeada y progresivamente invadida por tejido de granulación , que reemplazará el infarto con una cicatriz fibrosa ( colágena ) (que son pasos típicos en la cicatrización de heridas ). El espacio intersticial (el espacio entre las células fuera de los vasos sanguíneos) puede estar infiltrado con glóbulos rojos .
Estas características pueden reconocerse en los casos en que no se restauró la perfusión; Los infartos reperfundidos pueden tener otras características, como la necrosis de las bandas de contracción .
Estas tablas ofrecen una descripción general de la histopatología observada en el infarto de miocardio por tiempo después de la obstrucción.
Por parámetros individuales
| Parámetros histológicos del miocardio (tinción HE) | Manifestación más temprana | Desarrollo completo | Disminución / desaparición | Imagen |
|---|---|---|---|---|
| Fibras estiradas / onduladas | 1-2 h |

|
||
| Necrosis coagulativa : hipereosinofilia citoplasmática | 1-3 h | 1-3 días; hipereosinofilia citoplasmática y pérdida de estrías | > 3 días: desintegración |

|
| Edema intersticial | 4 a 12 h |
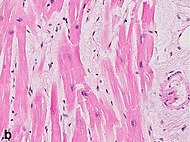
|
||
| Necrosis coagulativa : 'cambios nucleares' | 12-24 (picnosis, cariorrexis) | 1-3 días (pérdida de núcleos) | Depende del tamaño del infarto |
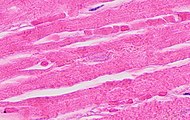
|
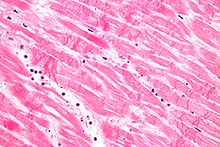
| Infiltración de neutrófilos | 12-24 h | 1-3 días | 5-7 días |
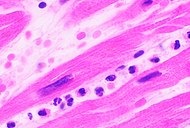
|
| Cariorrexis de neutrófilos | 1,5 a 2 días | 3-5 días |
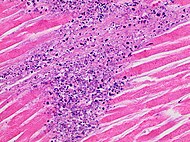
|
|
| Macrófagos y linfocitos | 3-5 días | 5 a 10 días (incluidos los 'siderófagos') | 10 días a 2 meses |

|
| Brotes vasculares / endoteliales * | 5 a 10 días | 10 días a 4 semanas | 4 semanas: desaparición de capilares; algunos vasos grandes dilatados persisten |
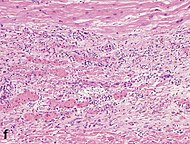
|
| Fibroblasto y colágeno joven * | 5 a 10 días | 2-4 semanas | Después de 4 semanas; depende del tamaño del infarto; |

|
| Fibrosis densa | 4 semanas | 2-3 meses | No |
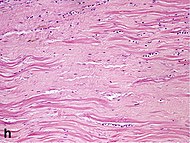
|
- Algunos autores resumen los cambios vasculares y fibróticos tempranos como 'tejido de granulación', que es máximo a las 2-3 semanas
Diagnósticos diferenciales de fibrosis miocárdica:
- La fibrosis intersticial , que es inespecífica, se ha descrito en insuficiencia cardíaca congestiva, hipertensión y envejecimiento normal.
- Fibrosis subepicárdica , que se asocia con diagnósticos distintos de infarto como miocarditis y miocardiopatía no isquémica.
Cronológico
| Tiempo | Examen macroscópico |
Histopatología por microscopía óptica |
|---|---|---|
| 0 - 0,5 horas | Ninguno | Ninguno |
| 0,5 - 4 horas | Ninguno |
|
| 4 - 12 horas |
|
|
| 12-24 horas |
|
|
| 13 días |
|
|
| 3-7 días |
|
|
| 7 - 10 días |
|
|
| 10-14 días |
|
|
| 2-8 semanas |
|
|
| Más de 2 meses | Cicatrización completa | Se formó una densa cicatriz de colágeno |
| Si no se especifica más en los recuadros, la referencia es nr | ||