Troponina - Troponin
La troponina , o el complejo de troponina , es un complejo de tres proteínas reguladoras ( troponina C , troponina I y troponina T ) que son parte integral de la contracción muscular en el músculo esquelético y el músculo cardíaco , pero no en el músculo liso . Las mediciones de las troponinas I y T específicas del corazón se utilizan ampliamente como indicadores de diagnóstico y pronóstico en el tratamiento del infarto de miocardio y el síndrome coronario agudo . Los niveles de troponina en sangre se pueden utilizar como marcador de diagnóstico de accidente cerebrovascular , aunque la sensibilidad de esta medición es baja.
Función
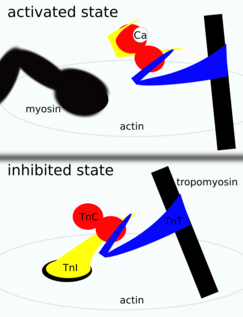
La troponina está unida a la proteína tropomiosina y se encuentra dentro del surco entre los filamentos de actina en el tejido muscular. En un músculo relajado, la tropomiosina bloquea el sitio de unión del puente cruzado de miosina , evitando así la contracción. Cuando la célula muscular es estimulada para contraerse por un potencial de acción , los canales de calcio se abren en la membrana sarcoplásmica y liberan calcio al sarcoplasma. Parte de este calcio se adhiere a la troponina, lo que hace que cambie de forma, exponiendo los sitios de unión de la miosina (sitios activos) en los filamentos de actina . La unión de la miosina a la actina provoca la formación de puentes cruzados y comienza la contracción del músculo.
La troponina se encuentra tanto en el músculo esquelético y el músculo cardíaco , pero las versiones específicas de troponina difieren entre los tipos de músculo. La principal diferencia es que la subunidad TnC de la troponina en el músculo esquelético tiene cuatro sitios de unión de iones de calcio, mientras que en el músculo cardíaco solo hay tres. No se ha establecido definitivamente la cantidad real de calcio que se une a la troponina.
Fisiología
Tanto en los músculos cardíacos como en los esqueléticos, la producción de fuerza muscular está controlada principalmente por cambios en la concentración de calcio intracelular . En general, cuando el calcio aumenta, los músculos se contraen y, cuando el calcio baja, los músculos se relajan.
La troponina es un componente de filamentos delgados (junto con la actina y la tropomiosina ) y es el complejo proteico al que se une el calcio para desencadenar la producción de fuerza muscular. La propia troponina tiene tres subunidades, TnC, TnI y TnT, cada una de las cuales desempeña un papel en la regulación de la fuerza. Bajo niveles intracelulares de calcio en reposo, la tropomiosina cubre los sitios activos de la actina a los que se une la miosina (un motor molecular organizado en filamentos musculares gruesos) para generar fuerza. Cuando el calcio se une a sitios específicos en el dominio N de la TnC, se produce una serie de cambios estructurales de la proteína de manera que la tropomiosina se separa de los sitios de unión de la miosina en la actina, lo que permite que la miosina se adhiera al filamento delgado y produzca fuerza y acorte la sarcómero .
Las subunidades individuales cumplen diferentes funciones:
- La troponina C se une a los iones de calcio para producir un cambio conformacional en TnI
- La troponina T se une a la tropomiosina, entrelazándolas para formar un complejo troponina-tropomiosina
- La troponina I se une a la actina en miofilamentos delgados para mantener el complejo actina-tropomiosina en su lugar
El músculo liso no tiene troponina.
Subunidades
TnT es una subunidad de unión a tropomiosina que regula la interacción del complejo de troponina con filamentos delgados; TnI inhibe la actividad de ATP-asa de acto-miosina; TnC es una subunidad de unión a Ca 2+ , que desempeña el papel principal en la regulación dependiente de Ca 2+ de la contracción muscular.
TnT y TnI en el músculo cardíaco se presentan en formas diferentes a las de los músculos esqueléticos. Dos isoformas de TnI y dos isoformas de TnT se expresan en tejido de músculo esquelético humano (skTnI y skTnT). Sólo se describe una isoforma de TnI específica de tejido para el tejido del músculo cardíaco (cTnI), mientras que la existencia de varias isoformas de TnT específicas del corazón (cTnT) se describe en la bibliografía. No se conocen isoformas cardíacas específicas para la TnC humana. La TnC en el tejido del músculo cardíaco humano se presenta mediante una isoforma típica del músculo esquelético lento. Otra forma de TnC, isoforma de TnC esquelética rápida, es más típica de los músculos esqueléticos rápidos. cTnI se expresa solo en el miocardio. No se conocen ejemplos de expresión de cTnI en músculo esquelético sano o lesionado o en otros tipos de tejido. La cTnT es probablemente menos específica para el corazón. Se ha descrito la expresión de cTnT en tejido esquelético de pacientes con lesiones crónicas del músculo esquelético.
Dentro del complejo de troponina cardíaca, se ha demostrado la interacción más fuerte entre moléculas para el complejo binario cTnI - TnC, especialmente en presencia de Ca 2+ (KA = 1.5x10 −8 M −1 ). TnC, formando un complejo con cTnI, cambia la conformación de la molécula de cTnI y protege parte de su superficie. Según los últimos datos, cTnI se libera en el torrente sanguíneo del paciente en forma de complejo binario con TnC o complejo ternario con cTnT y TnC. La formación del complejo cTnI-TnC juega un papel positivo importante en la mejora de la estabilidad de la molécula de cTnI. cTnI, que es extremadamente inestable en su forma libre, demuestra una estabilidad significativamente mejor en el complejo con TnC o en el complejo cTnI-cTnT-TnC ternario. Se ha demostrado que la estabilidad de cTnI en complejos nativos es significativamente mejor que la estabilidad de la forma purificada de la proteína o la estabilidad de cTnI en complejos de troponina artificiales combinados a partir de proteínas purificadas.
Investigar
Condiciones cardiacas
Ciertos subtipos de troponina ( I y T cardíacas ) son indicadores sensibles y específicos de daño al músculo cardíaco ( miocardio ). Se miden en la sangre para diferenciar entre angina inestable e infarto de miocardio (ataque cardíaco) en personas con dolor de pecho o síndrome coronario agudo . Una persona que recientemente tuvo un infarto de miocardio tendría un área de músculo cardíaco dañado y niveles elevados de troponina cardíaca en la sangre. Esto también puede ocurrir en personas con vasoespasmo coronario , un tipo de infarto de miocardio que involucra una constricción severa de los vasos sanguíneos cardíacos. Después de un infarto de miocardio, las troponinas pueden permanecer altas hasta por 2 semanas.
Las troponinas cardíacas son un marcador de todo el daño del músculo cardíaco, no solo del infarto de miocardio, que es la forma más grave de trastorno cardíaco. Sin embargo, la OMS establece actualmente los criterios de diagnóstico para la troponina elevada que indica infarto de miocardio en un umbral de 2 μg o más. Los niveles críticos de otros biomarcadores cardíacos también son relevantes, como la creatina quinasa . Otras condiciones que directa o indirectamente conducen al daño del músculo cardíaco y a la muerte también pueden aumentar los niveles de troponina, como la insuficiencia renal . La taquicardia severa (por ejemplo, debido a taquicardia supraventricular ) en un individuo con arterias coronarias normales también puede conducir a un aumento de troponinas, por ejemplo, se presume debido a una mayor demanda de oxígeno y un suministro inadecuado al músculo cardíaco.
Las troponinas también aumentan en pacientes con insuficiencia cardíaca , donde también predicen mortalidad y anomalías del ritmo ventricular. Pueden aumentar en afecciones inflamatorias como miocarditis y pericarditis con compromiso del músculo cardíaco (que luego se denomina miopericarditis). Las troponinas también pueden indicar varias formas de miocardiopatía , como miocardiopatía dilatada , miocardiopatía hipertrófica o hipertrofia ventricular (izquierda) , miocardiopatía periparto , miocardiopatía de Takotsubo o trastornos infiltrativos como la amiloidosis cardíaca .
Lesión del corazón con el aumento de las troponinas también se produce en contusión cardiaca , desfibrilación e interna o externa cardioversión . Las troponinas suelen aumentar en varios procedimientos, como la cirugía cardíaca y el trasplante de corazón , el cierre de los defectos del tabique auricular , la intervención coronaria percutánea o la ablación por radiofrecuencia .
Condiciones no cardíacas
La distinción entre afecciones cardíacas y no cardíacas es algo artificial; Las condiciones que se enumeran a continuación no son enfermedades cardíacas primarias, pero ejercen efectos indirectos sobre el músculo cardíaco.
Las troponinas aumentan en alrededor del 40% de los pacientes con enfermedades críticas como la sepsis . Existe un mayor riesgo de mortalidad y duración de la estancia en la unidad de cuidados intensivos en estos pacientes. En la hemorragia gastrointestinal grave , también puede haber un desajuste entre la demanda de oxígeno y el suministro del miocardio.
Los agentes de quimioterapia pueden ejercer efectos tóxicos en el corazón (los ejemplos incluyen antraciclina , ciclofosfamida , 5-fluorouracilo y cisplatino ). Varias toxinas y venenos también pueden provocar lesiones en el músculo cardíaco ( veneno de escorpión , veneno de serpiente y veneno de medusas y ciempiés ). El envenenamiento por monóxido de carbono o cianuro también puede ir acompañado de liberación de troponinas debido a efectos cardiotóxicos hipóxicos. La lesión cardíaca ocurre en aproximadamente un tercio de los casos graves de intoxicación por CO, y la detección de troponina es apropiada en estos pacientes.
En tanto primaria hipertensión pulmonar , embolia pulmonar , y las exacerbaciones agudas de la enfermedad pulmonar obstructiva crónica (EPOC), del ventrículo derecho resultados de deformación en el aumento de tensión de la pared y puede causar isquemia. Por supuesto, los pacientes con exacerbaciones de la EPOC también pueden tener un infarto de miocardio o una embolia pulmonar concurrentes, por lo que se debe tener cuidado de atribuir el aumento de los niveles de troponina a la EPOC.
Las personas con enfermedad renal en etapa terminal pueden tener niveles crónicamente elevados de troponina T, que están relacionados con un pronóstico más precario. Es menos probable que la troponina I esté falsamente elevada.
El ejercicio de resistencia extenuante , como maratones o triatlones, puede provocar un aumento de los niveles de troponina en hasta un tercio de los sujetos, pero no está relacionado con efectos adversos para la salud en estos competidores. También se han informado niveles altos de troponina T en pacientes con enfermedades musculares inflamatorias como polimiositis o dermatomiositis . Las troponinas también aumentan en la rabdomiólisis .
En los trastornos hipertensivos del embarazo, como la preeclampsia , los niveles elevados de troponina indican algún grado de daño miofibrilar.
La troponina T e I cardíaca se pueden utilizar para controlar la toxicidad de los cardiomiocitos inducida por fármacos y toxinas. .
En 2020, se encontró que los pacientes con COVID-19 con enfermedad grave tenían niveles más altos de troponina I en comparación con aquellos con enfermedad más leve.
Uso pronóstico
Los niveles elevados de troponina son importantes para el pronóstico en muchas de las condiciones en las que se utilizan para el diagnóstico.
En un estudio de cohorte basado en la comunidad que indica la importancia del daño cardíaco silencioso, se ha demostrado que la troponina I predice la mortalidad y el primer evento de enfermedad coronaria en hombres libres de enfermedad cardiovascular al inicio del estudio. En las personas con accidente cerebrovascular, los niveles elevados de troponina en sangre no son un marcador útil para detectar la afección.
Subunidades
La primera cTnI y más tarde la cTnT se utilizaron originalmente como marcadores de muerte de células cardíacas. Ambas proteínas se utilizan ahora ampliamente para diagnosticar infarto agudo de miocardio (IAM), angina inestable, traumatismo miocárdico posoperatorio y algunas otras enfermedades relacionadas con la lesión del músculo cardíaco. Ambos marcadores pueden detectarse en la sangre del paciente 3 a 6 horas después del inicio del dolor torácico, alcanzando el nivel máximo en 16 a 30 horas. La concentración elevada de cTnI y cTnT en muestras de sangre puede detectarse incluso 5-8 días después del inicio de los síntomas, lo que hace que ambas proteínas sean útiles también para el diagnóstico tardío de IAM.
Detección
La troponina T e I cardíaca se miden mediante métodos de inmunoensayo .
- Debido a las regulaciones de patentes, un solo fabricante ( Roche Diagnostics ) distribuye cTnT .
- Una gran cantidad de empresas de diagnóstico hacen que los métodos de inmunoensayo de cTnI estén disponibles en muchas plataformas de inmunoensayo diferentes.
La elevación de troponina después de la necrosis de células cardíacas comienza en 2-3 horas, alcanza su punto máximo en aprox. 24 horas y persiste durante 1 a 2 semanas.
Ver también
Referencias
enlaces externos
- Troponina en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- Troponinas en pruebas de laboratorio en línea