Condensación de Claisen - Claisen condensation
| Condensación de Claisen | |
|---|---|
| Lleva el nombre de | Rainer Ludwig Claisen |
| Tipo de reacción | Reacción de acoplamiento |
| Identificadores | |
| Portal de química orgánica | condensación claisen |
| ID de ontología RSC | RXNO: 0000043 |
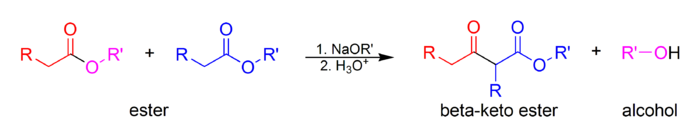
La condensación de Claisen es una reacción de formación de enlaces carbono-carbono que se produce entre dos ésteres o un éster y otro compuesto de carbonilo en presencia de una base fuerte , lo que da como resultado un β-ceto éster o una β- dicetona . Lleva el nombre de Rainer Ludwig Claisen , quien publicó por primera vez su trabajo sobre la reacción en 1887.
Requisitos
Al menos uno de los reactivos debe ser enolizable (tener un protón α y poder someterse a una desprotonación para formar el anión enolato ). Hay varias combinaciones diferentes de compuestos de carbonilo enolizables y no enolizables que forman algunos tipos diferentes de Claisen.
La base utilizada no debe interferir con la reacción al sufrir sustitución nucleofílica o adición con un carbono carbonilo. Por esta razón, la base de alcóxido de sodio conjugado del alcohol formado (por ejemplo, etóxido de sodio si se forma etanol ) se usa a menudo, ya que el alcóxido se regenera. En condensaciones de Claisen mixtas , se puede usar una base no nucleófila tal como diisopropilamida de litio , o LDA, ya que solo un compuesto es enolizable. El LDA no se usa comúnmente en las condensaciones clásicas de Claisen o Dieckmann debido a la enolización del éster electrófilo .
La porción alcoxi del éster debe ser un grupo saliente relativamente bueno . Los ésteres metílicos y etílicos , que producen metóxido y etóxido, respectivamente, se utilizan comúnmente.
Tipos
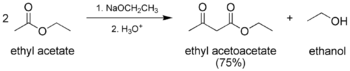
- La clásica condensación de Claisen, una autocondensación entre dos moléculas de un compuesto que contiene un éster enolizable.
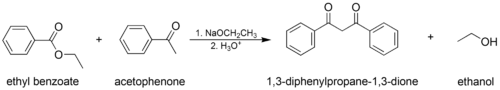
- La condensación de Claisen mixta (o "cruzada"), en la que se utilizan un éster o cetona enolizable y un éster no enolizable.
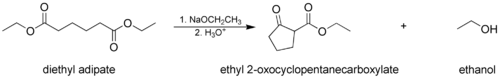
- La condensación de Dieckmann , donde una molécula con dos grupos éster reacciona intramolecularmente , formando un β-ceto éster cíclico . En este caso, el anillo formado no debe tensarse , normalmente una cadena o anillo de 5 o 6 miembros.
Mecanismo
En el primer paso del mecanismo, un protón α es eliminado por una base fuerte, lo que da como resultado la formación de un anión enolato, que se vuelve relativamente estable por la deslocalización de electrones. A continuación, el carbono carbonilo del (otro) éster es atacado nucleofílicamente por el anión enolato. A continuación, se elimina el grupo alcoxi (dando como resultado la (re) generación del alcóxido), y el alcóxido elimina el protón doblemente α recién formado para formar un nuevo anión enolato altamente estabilizado por resonancia. Se añade ácido acuoso (p. Ej., Ácido sulfúrico o ácido fosfórico ) en el paso final para neutralizar el enolato y cualquier base aún presente. A continuación, se aísla el β-cetoéster o β-dicetona recién formado. Nótese que la reacción requiere una cantidad estequiométrica de base ya que la eliminación del protón doblemente α impulsa termodinámicamente la reacción que de otro modo sería endergónica . Es decir, la condensación de Claisen no funciona con sustratos que tienen solo un α-hidrógeno debido al efecto de fuerza impulsora de la desprotonación del β-cetoéster en el último paso.
|
| animación |
Condensación de Stobbe
La condensación de Stobbe es una modificación específica para el éster dietílico del ácido succínico que requiere bases menos fuertes. Un ejemplo es su reacción con benzofenona :
Un mecanismo de reacción que explica la formación tanto de un grupo éster como de un grupo de ácido carboxílico se centra en un intermedio de lactona ( 5 ):
La condensación de Stobbe se utilizó en el primer paso de la síntesis de tametralina de Reinhard Sarges y también se puede utilizar en la síntesis de dimefadano .
Ver también
Referencias
enlaces externos
- "Condensación de Claisen" . Portal de Química Orgánica.