Peróxido de sodio - Sodium peroxide

|
|
|
|

|
|
| Nombres | |
|---|---|
| Otros nombres
Dióxido de disodio
Flocool Solozone Peróxido de disodio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| Tarjeta de información ECHA |
100.013.828 |
| Número CE | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| un numero | 1504 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| Na 2 O 2 | |
| Masa molar | 77,98 g / mol |
| Apariencia | polvo amarillo a blanco |
| Densidad | 2,805 g / cm 3 |
| Punto de fusion | 460 ° C (860 ° F; 733 K) (se descompone) |
| Punto de ebullición | 657 ° C (1215 ° F; 930 K) (se descompone) |
| reacciona violentamente | |
| Solubilidad | soluble en ácido insoluble en base reacciona con etanol |
| −28,10 · 10 −6 cm 3 / mol | |
| Estructura | |
| hexagonal | |
| Termoquímica | |
|
Capacidad calorífica ( C )
|
89,37 J / (mol · K) |
|
Entropía molar estándar ( S |
95 J / (mol · K) |
| −515 kJ · mol −1 | |
|
Energía libre de Gibbs (Δ f G ˚)
|
−446,9 kJ / mol |
| Riesgos | |
| Ficha de datos de seguridad | MSDS externa |
|
|
|
| Frases R (desactualizadas) | R8 , R35 |
| Frases S (desactualizadas) | (S1 / 2) , S8 , S27 , S39 , S45 |
| NFPA 704 (diamante de fuego) | |
| punto de inflamabilidad | No es inflamable |
| Compuestos relacionados | |
|
Otros cationes
|
Peróxido de litio Peróxido de potasio Peróxido de rubidio Peróxido de cesio |
|
Óxido de sodio Superóxido de sodio |
|
|
Compuestos relacionados
|
Hidróxido de sodio Peróxido de hidrógeno |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El peróxido de sodio es el compuesto inorgánico con la fórmula Na 2 O 2 . Este sólido amarillento es producto del sodio encendido en exceso de oxígeno. Es una base fuerte. Este peróxido de metal existe en varios hidratos y peroxihidratos, incluidos Na 2 O 2 · 2H 2 O 2 · 4H 2 O, Na 2 O 2 · 2H 2 O, Na 2 O 2 · 2H 2 O 2 y Na 2 O 2 · 8H 2 O. El octahidrato, que es fácil de preparar, es blanco, en contraste con el material anhidro.
Propiedades
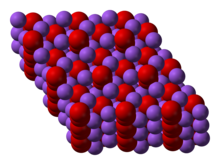
El peróxido de sodio cristaliza con simetría hexagonal. Al calentarse, la forma hexagonal experimenta una transición a una fase de simetría desconocida a 512 ° C. Con un calentamiento adicional por encima del punto de ebullición de 657 ° C, el compuesto se descompone en Na 2 O, liberando O 2 .
- 2 Na 2 O 2 → 2 Na 2 O + O 2
Preparación
El octahidrato se produce tratando hidróxido de sodio con peróxido de hidrógeno.
El peróxido de sodio se puede preparar a gran escala mediante la reacción de sodio metálico con oxígeno a 130-200 ° C, un proceso que genera óxido de sodio , que en una etapa separada absorbe oxígeno:
- 4 Na + O 2 → 2 Na 2 O
- 2 Na 2 O + O 2 → 2 Na 2 O 2
También se puede producir pasando gas ozono sobre yoduro de sodio sólido dentro de un tubo de platino o paladio . El ozono oxida el sodio para formar peróxido de sodio. El yodo se puede sublimar con un calentamiento suave. El platino o paladio cataliza la reacción y no es atacado por el peróxido de sodio.
Usos
El peróxido de sodio se hidroliza para dar hidróxido de sodio y peróxido de hidrógeno según la reacción.
- Na 2 O 2 + 2 H 2 O → 2 NaOH + H 2 O 2
El peróxido de sodio se utilizó para blanquear la pulpa de madera para la producción de papel y textiles. Actualmente se utiliza principalmente para operaciones de laboratorio especializadas, por ejemplo, la extracción de minerales de varios minerales. El peróxido de sodio puede tener los nombres comerciales de Solozone y Flocool . En las preparaciones químicas, el peróxido de sodio se usa como agente oxidante. También se utiliza como fuente de oxígeno al reaccionar con dióxido de carbono para producir oxígeno y carbonato de sodio:
- 2 Na 2 O 2 + 2 CO 2 → 2 Na 2 CO 3 + O 2
Por tanto, es particularmente útil en equipos de buceo, submarinos, etc. El peróxido de litio y el superóxido de potasio tienen usos similares.

