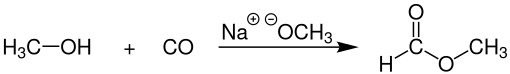Formiato de metilo - Methyl formate
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC preferido
Formiato de metilo |
|||
|
Nombre IUPAC sistemático
Metanoato de metilo |
|||
| Otros nombres
R-611
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| Tarjeta de información ECHA | 100.003.166 | ||
|
PubChem CID
|
|||
| UNII | |||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| C 2 H 4 O 2 | |||
| Masa molar | 60,052 g · mol −1 | ||
| Apariencia | Líquido incoloro | ||
| Olor | agradable | ||
| Densidad | 0,98 g / cm 3 | ||
| Punto de fusion | −100 ° C (−148 ° F; 173 K) | ||
| Punto de ebullición | 32 ° C (90 ° F; 305 K) | ||
| 30% (20 ° C) | |||
| Presión de vapor | 634 hPa (476 mmHg) (20 ° C) | ||
| -32,0 · 10 −6 cm 3 / mol | |||
| Peligros | |||
| Ficha de datos de seguridad | MSDS de Oxford | ||
| Altamente inflamable (F +); Dañino (Xn) | |||
| punto de inflamabilidad | -19 ° C; −2 ° F; 254 K | ||
| Límites explosivos | 4,5% -23% | ||
| Dosis o concentración letal (LD, LC): | |||
|
LD 50 ( dosis mediana )
|
1622 mg / kg (oral, conejo) | ||
|
LC Lo ( menor publicado )
|
50.000 ppm (conejillo de indias, 20 min) | ||
| NIOSH (límites de exposición a la salud de EE. UU.): | |||
|
PEL (permitido)
|
TWA 100 ppm (250 mg / m 3 ) | ||
|
REL (recomendado)
|
TWA 100 ppm (250 mg / m 3 ) ST 150 ppm (375 mg / m 3 ) | ||
|
IDLH (peligro inmediato)
|
4500 ppm | ||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
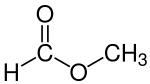
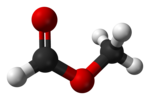
El formiato de metilo , también llamado metanoato de metilo , es el éster metílico del ácido fórmico . El ejemplo más simple de un éster, es un líquido incoloro con un olor etéreo, alta presión de vapor y baja tensión superficial . Es un precursor de muchos otros compuestos de interés comercial.
Producción
En el laboratorio, el formiato de metilo se puede producir mediante la reacción de condensación del metanol y el ácido fórmico , de la siguiente manera:
- HCOOH + CH 3 OH → HCO 2 CH 3 + H 2 O
Sin embargo, el formiato de metilo industrial generalmente se produce mediante la combinación de metanol y monóxido de carbono ( carbonilación ) en presencia de una base fuerte, como el metóxido de sodio :
Este proceso, practicado comercialmente por BASF entre otras empresas, proporciona una selectividad del 96% hacia el formiato de metilo. El catalizador para este proceso es sensible al agua, que puede estar presente en la materia prima de monóxido de carbono , que comúnmente se deriva del gas de síntesis . El monóxido de carbono muy seco es, por tanto, esencial.
Usos
El formiato de metilo se usa principalmente para fabricar formamida , dimetilformamida y ácido fórmico . Estos compuestos son precursores o componentes básicos de muchos derivados útiles.
Debido a su alta presión de vapor , se utiliza para acabados de secado rápido y como agente de expansión para algunas aplicaciones de espuma de poliuretano y como reemplazo de CFC , HCFC y HFC . El formiato de metilo tiene cero potencial de agotamiento del ozono y cero potencial de calentamiento global . También se utiliza como insecticida .
Un uso histórico del formiato de metilo, que a veces llama la atención, fue en refrigeración. Antes de la introducción de refrigerantes menos tóxicos, el formiato de metilo se utilizaba como alternativa al dióxido de azufre en los refrigeradores domésticos, como algunos modelos del famoso GE Monitor Top.