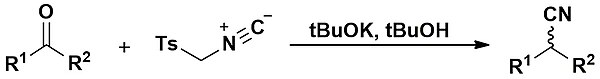Reacción de Van Leusen - Van Leusen reaction
| Reacción de Van Leusen | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Lleva el nombre de | Daan Van Leusen Albert M. Van Leusen |
||||||||
| Tipo de reacción | Reacción de sustitución | ||||||||
| Reacción | |||||||||
|
|||||||||
| Identificadores | |||||||||
| Portal de química orgánica | reacción de van-leusen | ||||||||
La reacción de Van Leusen es la reacción de una cetona con TosMIC que conduce a la formación de un nitrilo . Fue descrito por primera vez en 1977 por Van Leusen y colaboradores. Cuando se emplean aldehídos , la reacción de Van Leusen es particularmente útil para formar oxazoles e imidazoles .
Mecanismo
El mecanismo de reacción consiste en la desprotonación inicial de TosMIC, que es fácil gracias al efecto de captación de electrones de los grupos sulfona e isocianuro . El ataque al carbonilo es seguido por una ciclación 5-endo-dig (siguiendo las reglas de Baldwin ) en un anillo de 5 miembros.
| Síntesis de oxazol de Van Leusen | |||||||
|---|---|---|---|---|---|---|---|
| Lleva el nombre de | Daan Van Leusen Albert M. Van Leusen |
||||||
| Tipo de reacción | Reacción de formación de anillo | ||||||
| Reacción | |||||||
|
|||||||
| Identificadores | |||||||
| Portal de química orgánica | síntesis de van-leusen-oxazol | ||||||
Si el sustrato es un aldehído, entonces puede ocurrir fácilmente la eliminación del excelente grupo saliente tosilo . Al apagar, la molécula resultante es un oxazol.
| Síntesis de imidazol de Van Leusen | |
|---|---|
| Lleva el nombre de | Daan Van Leusen Albert M. Van Leusen |
| Tipo de reacción | Reacción de formación de anillo |
| Identificadores | |
| Portal de química orgánica | síntesis de van-leusen-imidazol |
Si se usa una aldimina , formada a partir de la condensación de un aldehído con una amina , se pueden generar imidazoles mediante el mismo proceso.
Cuando se usan cetonas en su lugar, la eliminación no puede ocurrir; más bien, un proceso de tautomerización da un intermedio que después de un proceso de apertura del anillo y la eliminación del grupo tosilo forma una alqueneimina N -formilada. A continuación, se solvoluciona con una solución de alcohol ácido para dar el producto de nitrilo.
Referencias
- ^ Van Leusen, Daan; Oldenziel, Otto; Van Leusen, Albert (1977). "Química de los isocianuros de sulfonilmetilo. 13. Una síntesis general en un solo paso de nitrilos a partir de cetonas usando isocianuro de tosilmetilo. Introducción de una unidad de un carbono". J. Org. Chem. Sociedad Química Estadounidense . 42 (19): 3114–3118. doi : 10.1021 / jo00439a002 .
- ^ Gracias, Vijaya; Gasiecki, Alan; Djuric, Stevan (2005). "Síntesis de imidazoles bicíclicos fusionados por reacciones de metátesis de cierre de anillo / Van Leusen secuenciales". Org. Letón. Sociedad Química Americana. 7 (15): 3183–3186. doi : 10.1021 / ol050852 + . PMID 16018616 .