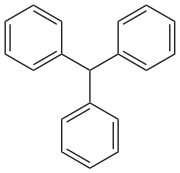
Trifenilmetano - Triphenylmethane
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
1,1 ′, 1 ′ ′ - Metanotriiltribenceno |
|
| Otros nombres
Trifenilmetano
1,1 ′, 1 ′ ′ - Metilidinetrisbenceno |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEBI | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.007.524 |
| Número CE | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 19 H 16 | |
| Masa molar | 244,337 g · mol −1 |
| Apariencia | Sólido incoloro |
| Densidad | 1,014 g / cm 3 |
| Punto de fusion | 92 a 94 ° C (198 a 201 ° F; 365 a 367 K) |
| Punto de ebullición | 359 ° C (678 ° F; 632 K) |
| Insoluble | |
| Solubilidad | Soluble en dioxano y hexano. |
| Acidez (p K a ) | 33,3 |
| −165,6 × 10 −6 cm 3 / mol | |
| Riesgos | |
| Ficha de datos de seguridad | MSDS externa |
| Frases R (desactualizadas) | R36 R37 R38 |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
Trifenilmetano , o metano de trifenilo , es el de hidrocarburos con la fórmula (C 6 H 5 ) 3 CH. Este sólido incoloro es soluble en solventes orgánicos apolares y no en agua. El trifenilmetano es el esqueleto básico de muchos tintes sintéticos llamados tintes de triarilmetano , muchos de ellos son indicadores de pH y algunos muestran fluorescencia . Un grupo tritilo en química orgánica es un grupo trifenilmetilo Ph 3 C, por ejemplo, cloruro de trifenilmetilo (cloruro de tritilo) y el radical trifenilmetilo (radical tritilo).
Preparación
El trifenilmetano fue sintetizado por primera vez en 1872 por el químico alemán August Kekulé y su estudiante belga Antoine Paul Nicolas Franchimont (1844-1919) calentando difenilmercurio (Hg (C 6 H 5 ) 2 , Quecksilberdifenilo ) con cloruro de benzal (C 6 H 5 CHCl 2 , Cloruro de bencilo ).
El trifenilmetano se puede sintetizar mediante la reacción de Friedel-Crafts a partir de benceno y cloroformo con un catalizador de cloruro de aluminio :
- 3 C 6 H 6 + CHCl 3 → Ph 3 CH + 3 HCl
Alternativamente, el benceno puede reaccionar con tetracloruro de carbono utilizando el mismo catalizador para obtener el cloruro de trifenilmetilo - cloruro de aluminio aducto, que se hidroliza con ácido diluido:
- 3 C 6 H 6 + CCl 4 + AlCl 3 → Ph 3 CCl · AlCl 3
- Ph 3 CCl · AlCl 3 + HCl → Ph 3 CH
También se utiliza la síntesis a partir de cloruro de bencilideno , preparado a partir de benzaldehído y pentacloruro de fósforo .
Reacciones del enlace CH
El p K a es 33,3. El trifenilmetano es significativamente más ácido que la mayoría de los otros hidrocarburos porque la carga está deslocalizada en tres anillos de fenilo. Sin embargo, los efectos estéricos impiden que los tres anillos de fenilo alcancen la coplanariedad simultáneamente. En consecuencia, el difenilmetano es aún más ácido, porque en su anión la carga se distribuye sobre dos anillos de fenilo al mismo tiempo. El anión tritilo es rojo. Este color se puede utilizar como indicador en valoraciones ácido-base .
La sal de sodio se puede preparar también a partir del cloruro :
- (C 6 H 5 ) 3 CCl + 2 Na → (C 6 H 5 ) 3 CNa + NaCl
El uso de tritilsodio como una base fuerte no nucleofílica ha sido eclipsado por la popularización del butillitio y bases fuertes relacionadas.
El enlace Ph 3 C-H es relativamente débil, con una energía de disociación del enlace (BDE) de 81 kcal / mol. Por el contrario, el BDE del metano es de 105 kcal / mol.
Colorantes de triarilmetano
Ejemplos de tintes de triarilmetano son el verde de bromocresol :
Y el verde malaquita que contiene nitrógeno :
Ver también
- Tetrafenilmetano
- Trifenilmetanol
- Cloruro de trifenilmetilo
- Hexafluorofosfato de trifenilmetilo
- Radical trifenilmetilo


