Indeno - Indene
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
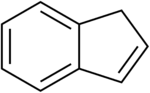
1 H- Indeno |
|
| Otros nombres
Benzociclopentadieno
Indonafteno Biciclo [4.3.0] nona-1,3,5,7-tetraeno |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 635873 | |
| CHEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Tarjeta de información ECHA |
100.002.176 |
| Número CE | |
| 27265 | |
| KEGG | |
|
PubChem CID
|
|
| UNII | |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 9 H 8 | |
| Masa molar | 116,16 |
| Apariencia | Líquido incoloro |
| Densidad | 0,997 g / ml |
| Punto de fusion | −1,8 ° C (28,8 ° F; 271,3 K) |
| Punto de ebullición | 181,6 ° C (358,9 ° F; 454,8 K) |
| Insoluble | |
| Acidez (p K a ) | 20,1 (en DMSO) |
| −80,89 × 10 −6 cm 3 / mol | |
| Peligros | |
| Principales peligros | Inflamable |
| punto de inflamabilidad | 78,3 ° C (172,9 ° F; 351,4 K) |
| NIOSH (límites de exposición a la salud de EE. UU.): | |
|
PEL (permitido)
|
ninguno |
|
REL (recomendado)
|
TWA 10 ppm (45 mg / m 3 ) |
|
IDLH (peligro inmediato)
|
DAKOTA DEL NORTE |
| Compuestos relacionados | |
|
Compuestos relacionados
|
Benzofurano , benzotiofeno , indol |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El indeno es un hidrocarburo policíclico inflamable con fórmula química C 9 H 8 . Está compuesto por un anillo de benceno fusionado con un anillo de ciclopenteno . Este líquido aromático es incoloro, aunque las muestras suelen ser de color amarillo pálido. El principal uso industrial del indeno es la producción de resinas termoplásticas de indeno / cumarona . Los indenos sustituidos y sus derivados indanos estrechamente relacionados son motivos estructurales importantes que se encuentran en muchos productos naturales y moléculas biológicamente activas , como el sulindaco .
Aislamiento
El indeno se encuentra de forma natural en las fracciones de alquitrán de hulla que hierven entre 175 y 185 ° C. Puede obtenerse calentando esta fracción con sodio para precipitar "sodio-indeno" sólido. Este paso aprovecha la débil acidez del indeno evidenciada por su desprotonación por sodio para dar el derivado de indenilo. El sodio-indeno se convierte de nuevo en indeno mediante destilación al vapor .
Reactividad
El indeno se polimeriza fácilmente . La oxidación del indeno con dicromato ácido produce ácido homoftálico ( ácido o -carboxilfenilacético ). Se condensa con oxalato de dietilo en presencia de etóxido de sodio para formar éster indeno-oxálico, y con aldehídos o cetonas en presencia de álcalis para formar benzofulvenos , que son muy coloreados. El tratamiento del indeno con reactivos de organolitio da compuestos de indenilo de litio :
- C 9 H 8 + RLi → Li C 9 H 7 + RH
El indenilo es un ligando en la química organometálica que da lugar a muchos complejos de indenilo de metales de transición .
Ver también
Referencias
- ^ Unión Internacional de Química Pura y Aplicada (2014). Nomenclatura de la química orgánica: Recomendaciones y nombres preferidos de la IUPAC 2013 . La Real Sociedad de Química . pag. 207. doi : 10.1039 / 9781849733069 . ISBN 978-0-85404-182-4.
- ^ a b c d Guía de bolsillo de NIOSH sobre peligros químicos. "# 0340" . Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Bordwell FG (1988). "Equilibrio de acidez en solución de dimetilsulfóxido". Cuentas de Investigación Química . 21 (12): 456–463. doi : 10.1021 / ar00156a004 . Bordwell pKa Table in DMSO Archivado el 9 de octubre de 2008 en la Wayback Machine.
- ^ Wu, Jie; Qiu, Guanyinsheng (2014). "Generación de derivados del indeno por reacciones en tándem". Synlett . 25 (19): 2703–2713. doi : 10.1055 / s-0034-1379318 .
- ^ Collin, Gerd; Mildenberg, Rolf; Zander, Mechthild; Höke, Hartmut; McKillip, William; Freitag, Werner; Imöhl, Wolfgang. "Resinas sintéticas". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH.
- ^ O'Connor, Joseph M .; Casey, Charles P. (1987). "Química de deslizamiento de anillo de complejos de ciclopentadienilo e indenilo de metales de transición". Revisiones químicas . 87 (2): 307–318. doi : 10.1021 / cr00078a002 .
enlaces externos
- W. contra Miller, Rohde (1890). "Zur Synthese von Indenderivaten" . Berichte der Deutschen Chemischen Gesellschaft . 23 (2): 1881–1886. doi : 10.1002 / cber.18900230227 .
- W. contra Miller, Rohde (1890). "Zur Synthese von Indenderivaten" . Berichte der Deutschen Chemischen Gesellschaft . 23 (2): 1887-1902. doi : 10.1002 / cber.18900230228 .
- Finar, IL (1985). Química Orgánica . Longman Scientific & Technical. ISBN 0-582-44257-5.
