Triptófano - Tryptophan

Fórmula esquelética de L- triptófano
|
|||
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC
Triptófano o ácido (2 S ) -2-amino-3- ( 1H -indol-3-il) propanoico
|
|||
| Otros nombres
Ácido 2-amino-3- ( 1H -indol-3-il) propanoico
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| CHEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Tarjeta de información ECHA |
100.000.723 |
||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
|
Tablero CompTox ( EPA )
|
|||
|
|||
| Propiedades | |||
| C 11 H 12 N 2 O 2 | |||
| Masa molar | 204,229 g · mol −1 | ||
| Soluble: 0,23 g / L a 0 ° C, 11,4 g / L a 25 ° C, |
|||
| Solubilidad | Soluble en alcohol caliente, hidróxidos alcalinos; insoluble en cloroformo . | ||
| Acidez (p K a ) | 2,38 (carboxilo), 9,39 (amino) | ||
| -132,0 · 10 −6 cm 3 / mol | |||
| Farmacología | |||
| N06AX02 ( OMS ) | |||
| Página de datos complementarios | |||
|
Índice de refracción ( n ), constante dieléctrica (ε r ), etc. |
|||
|
Datos termodinámicos |
Comportamiento de fase sólido-líquido-gas |
||
| UV , IR , RMN , MS | |||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
El triptófano (símbolo Trp o W ) es un α- aminoácido que se utiliza en la biosíntesis de proteínas . El triptófano contiene un grupo α-amino, un grupo de ácido α- carboxílico y un indol de cadena lateral , lo que lo convierte en un aminoácido aromático no polar . Es esencial en el ser humano, lo que significa que el cuerpo no puede sintetizarlo y debe obtenerse de la dieta. El triptófano también es un precursor del neurotransmisor serotonina , la hormona melatonina y la vitamina B3 . Está codificado por el codón UGG.
Como otros aminoácidos, el triptófano es un ion híbrido a pH fisiológico donde el grupo amino está protonado (- NH+
3; pK a = 9,39) y el ácido carboxílico se desprotona (–COO - ; pK a = 2,38).
Función
Los aminoácidos, incluido el triptófano, se utilizan como componentes básicos en la biosíntesis de proteínas , y las proteínas son necesarias para mantener la vida. Muchos animales (incluidos los humanos) no pueden sintetizar triptófano: necesitan obtenerlo a través de su dieta, lo que lo convierte en un aminoácido esencial . El triptófano es uno de los aminoácidos menos comunes que se encuentran en las proteínas, pero juega un papel estructural o funcional importante siempre que ocurre. Por ejemplo, los residuos de triptófano y tirosina juegan un papel especial en el "anclaje" de las proteínas de la membrana dentro de la membrana celular . El triptófano, junto con otros aminoácidos aromáticos , también es importante en las interacciones glucano-proteína . Además, el triptófano funciona como precursor bioquímico de los siguientes compuestos :
- Serotonina (un neurotransmisor ), sintetizada por triptófano hidroxilasa .
- La melatonina (una neurohormona ) se sintetiza a su vez a partir de la serotonina, a través de las enzimas N-acetiltransferasa y 5-hidroxiindol-O-metiltransferasa .
- Cinurenina , a la que se metaboliza principalmente el triptófano (más del 95%). Dos enzimas, a saber, la indolamina 2,3-dioxigenasa (IDO) en el sistema inmunológico y el cerebro, y la triptófano dioxigenasa (TDO) en el hígado, son responsables de la síntesis de quinurenina a partir del triptófano. La vía de la quinurenina del catabolismo del triptófano está alterada en varias enfermedades, incluidos los trastornos psiquiátricos como la esquizofrenia, el trastorno depresivo mayor y el trastorno bipolar.
- La niacina , también conocida como vitamina B 3 , se sintetiza a partir del triptófano a través de quinurenina y ácidos quinolínicos .
- Las auxinas (una clase de fitohormonas ) se sintetizan a partir del triptófano.
El trastorno de mala absorción de fructosa causa una absorción inadecuada de triptófano en el intestino, niveles reducidos de triptófano en la sangre y depresión.
En las bacterias que sintetizan triptófano, los altos niveles celulares de este aminoácido activan una proteína represora , que se une al operón trp . La unión de este represor al operón triptófano evita la transcripción del ADN corriente abajo que codifica las enzimas implicadas en la biosíntesis del triptófano. Por lo tanto, los niveles altos de triptófano impiden la síntesis de triptófano a través de un circuito de retroalimentación negativa , y cuando los niveles de triptófano de la célula vuelven a bajar, se reanuda la transcripción del operón trp. Esto permite respuestas rápidas y estrictamente reguladas a los cambios en los niveles de triptófano internos y externos de la célula.
|
El metabolismo del triptófano por la microbiota gastrointestinal humana (
)
|
Cantidad diaria recomendada
En 2002, el Instituto de Medicina de EE. UU. Estableció una cantidad diaria recomendada (RDA) de 5 mg / kg de peso corporal / día de triptófano para adultos de 19 años o más.
Fuentes dietéticas
El triptófano está presente en la mayoría de los alimentos a base de proteínas o en las proteínas dietéticas. Es particularmente abundantes en el chocolate , avena , secas fechas , leche , yogur , queso cottage , carne roja , huevos , pescado , aves de corral , de sésamo , garbanzos , almendras , semillas de girasol , semillas de calabaza , trigo sarraceno , la espirulina , y los cacahuetes . Contrariamente a la creencia popular de que el pavo cocido contiene una gran cantidad de triptófano, el contenido de triptófano en el pavo es típico de las aves de corral.
| Comida | Triptófano [g / 100 g de alimento] |
Proteína [g / 100 g de alimento] |
Triptófano / proteína [%] |
|---|---|---|---|
| Clara de huevo seca | 1,00 | 81,10 | 1,23 |
| Espirulina , seca | 0,92 | 57,47 | 1,62 |
| Bacalao atlántico seco | 0,70 | 62,82 | 1,11 |
| Soja , cruda | 0,59 | 36,49 | 1,62 |
| Queso, parmesano | 0,56 | 37,90 | 1,47 |
| Semillas de chía , secas | 0.436 | 16,5 | 2,64 |
| semilla de sésamo | 0,37 | 17.00 | 2.17 |
| Queso, Cheddar | 0,32 | 24,90 | 1,29 |
| Semilla de girasol | 0,30 | 17.20 | 1,74 |
| Chuleta de cerdo | 0,25 | 19.27 | 1,27 |
| pavo | 0,24 | 21,89 | 1,11 |
| Pollo | 0,24 | 20,85 | 1,14 |
| Carne de res | 0,23 | 20.13 | 1.12 |
| Avena | 0,23 | 16,89 | 1,39 |
| Salmón | 0,22 | 19,84 | 1.12 |
| Cordero, chuleta | 0,21 | 18.33 | 1,17 |
| Perca, Atlántico | 0,21 | 18,62 | 1.12 |
| Garbanzos , crudos | 0,19 | 19.30 | 0,96 |
| Huevo | 0,17 | 12.58 | 1,33 |
| Harina de trigo, blanca | 0,13 | 10,33 | 1,23 |
| Chocolate para hornear , sin azúcar | 0,13 | 12,9 | 1,23 |
| Leche | 0,08 | 3,22 | 2,34 |
| Arroz, blanco, de grano medio, cocido | 0,028 | 2,38 | 1,18 |
| Quinua , cruda | 0,167 | 14.12 | 1.2 |
| Quinua, cocida | 0.052 | 4,40 | 1.1 |
| Patatas, rojizas | 0,02 | 2.14 | 0,84 |
| Tamarindo | 0,018 | 2,80 | 0,64 |
| Banana | 0,01 | 1.03 | 0,87 |
Usar como antidepresivo
Debido a que el triptófano se convierte en 5-hidroxitriptófano (5-HTP) que luego se convierte en el neurotransmisor serotonina, se ha propuesto que el consumo de triptófano o 5-HTP puede mejorar los síntomas de depresión al aumentar el nivel de serotonina en el cerebro. El triptófano se vende sin receta en los Estados Unidos (después de haber sido prohibido en diversos grados entre 1989 y 2005 ) y el Reino Unido como suplemento dietético para su uso como antidepresivo , ansiolítico y ayuda para dormir . También se comercializa como medicamento recetado en algunos países europeos para el tratamiento de la depresión mayor . Existe evidencia de que es poco probable que los niveles de triptófano en sangre se alteren al cambiar la dieta, pero el consumo de triptófano purificado aumenta el nivel de serotonina en el cerebro, mientras que el consumo de alimentos que contienen triptófano no lo hace. Esto se debe a que el sistema de transporte que lleva el triptófano a través de la barrera hematoencefálica también transporta otros aminoácidos que se encuentran en las fuentes de alimentos proteicos . Los niveles elevados en plasma sanguíneo de otros aminoácidos neutros grandes evitan que la concentración plasmática de triptófano aumente los niveles de concentración cerebral.
En 2001 se publicó una revisión Cochrane del efecto del 5-HTP y el triptófano sobre la depresión. Los autores incluyeron solo estudios de alto rigor e incluyeron tanto el 5-HTP como el triptófano en su revisión debido a los datos limitados sobre ambos. De 108 estudios de 5-HTP y triptófano sobre la depresión publicados entre 1966 y 2000, solo dos cumplieron con los estándares de calidad de los autores para su inclusión, con un total de 64 participantes del estudio. Las sustancias fueron más efectivas que el placebo en los dos estudios incluidos, pero los autores afirman que "la evidencia fue de calidad insuficiente para ser concluyente" y señalan que "debido a que existen antidepresivos alternativos que han demostrado ser efectivos y seguros, la utilidad clínica de El 5-HTP y el triptófano están limitados en la actualidad ". El uso de triptófano como terapia complementaria además del tratamiento estándar para los trastornos del estado de ánimo y la ansiedad no está respaldado por evidencia científica.
Efectos secundarios
Los posibles efectos secundarios de la suplementación con triptófano incluyen náuseas , diarrea , somnolencia , aturdimiento , dolor de cabeza , boca seca , visión borrosa , sedación , euforia y nistagmo (movimientos oculares involuntarios).
Interacciones
El triptófano tomado como suplemento dietético (como en forma de tableta) tiene el potencial de causar síndrome serotoninérgico cuando se combina con antidepresivos de la clase IMAO o ISRS u otros fármacos fuertemente serotoninérgicos. Debido a que la suplementación con triptófano no se ha estudiado a fondo en un entorno clínico, sus interacciones con otros medicamentos no se conocen bien.
Aislamiento
El aislamiento de triptófano fue informado por primera vez por Frederick Hopkins en 1901. Hopkins recuperó el triptófano de la caseína hidrolizada , recuperando 4-8 g de triptófano de 600 g de caseína cruda.
Biosíntesis y producción industrial
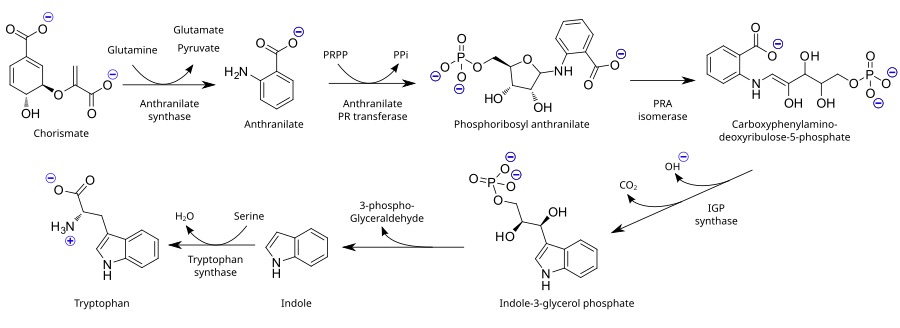
Como aminoácido esencial, el triptófano no se sintetiza a partir de sustancias más simples en humanos y otros animales, por lo que debe estar presente en la dieta en forma de proteínas que contienen triptófano. Las plantas y los microorganismos comúnmente sintetizan triptófano a partir del ácido shikímico o antranilato : el antranilato se condensa con fosforribosilpirofosfato (PRPP), generando pirofosfato como subproducto. El anillo del resto de ribosa se abre y se somete a descarboxilación reductora , produciendo indol-3-glicerol fosfato; esto, a su vez, se transforma en indol . En el último paso, la triptófano sintasa cataliza la formación de triptófano a partir del indol y el aminoácido serina .
La producción industrial de triptófano también es biosintética y se basa en la fermentación de serina e indol utilizando bacterias de tipo salvaje o genéticamente modificadas como B. amyloliquefaciens , B. subtilis , C. glutamicum o E. coli . Estas cepas portan mutaciones que impiden la recaptación de aminoácidos aromáticos o operones trp múltiples / sobreexpresados . La conversión es catalizada por la enzima triptófano sintasa .
sociedad y Cultura
Síndrome de eosinofilia-mialgia
Hubo un gran brote de síndrome de eosinofilia-mialgia (EMS) en los EE. UU. En 1989, con más de 1,500 casos reportados a los CDC y al menos 37 muertes. Después de que una investigación preliminar reveló que el brote estaba relacionado con la ingesta de triptófano, la Administración de Drogas y Alimentos de los EE. UU . (FDA) retiró los suplementos de triptófano en 1989 y prohibió la mayoría de las ventas públicas en 1990, y otros países siguieron su ejemplo.
Estudios posteriores sugirieron que EMS estaba vinculado a lotes específicos de L-triptófano suministrados por un solo gran fabricante japonés, Showa Denko . Finalmente, quedó claro que los lotes recientes de L-triptófano de Showa Denko estaban contaminados por trazas de impurezas, que posteriormente se pensó que eran responsables del brote de EMS de 1989. Sin embargo, otra evidencia sugiere que el triptófano en sí mismo puede ser un factor contribuyente potencialmente importante en EMS.
La FDA relajó sus restricciones sobre las ventas y la comercialización de triptófano en febrero de 2001, pero continuó limitando la importación de triptófano no destinado a un uso exento hasta 2005.
El hecho de que las instalaciones de Showa Denko utilizaran bacterias modificadas genéticamente para producir los lotes contaminados de L-triptófano que posteriormente se descubrió que habían causado el brote del síndrome de eosinofilia-mialgia se ha citado como evidencia de la necesidad de "un seguimiento estrecho de la pureza química de la biotecnología". -productos derivados ". Aquellos que piden un monitoreo de la pureza, a su vez, han sido criticados como activistas anti- OGM que pasan por alto las posibles causas de contaminación no OGM y amenazan el desarrollo de la biotecnología.
Carne de pavo y somnolencia.
Una afirmación común en los EE. UU. Es que el consumo excesivo de carne de pavo produce somnolencia , debido a los altos niveles de triptófano que contiene el pavo. Sin embargo, la cantidad de triptófano en el pavo es comparable a la que contienen otras carnes. La somnolencia después de comer puede ser causada por otros alimentos que se comen con el pavo, en particular los carbohidratos . La ingestión de una comida rica en carbohidratos desencadena la liberación de insulina . La insulina, a su vez, estimula la captación de grandes aminoácidos de cadena ramificada neutra (BCAA), pero no triptófano, en el músculo, aumentando la proporción de triptófano a BCAA en el torrente sanguíneo. El aumento de la proporción de triptófano resultante reduce la competencia en el gran transportador de aminoácidos neutros (que transporta tanto BCAA como aminoácidos aromáticos), lo que da como resultado una mayor captación de triptófano a través de la barrera hematoencefálica hacia el líquido cefalorraquídeo (LCR). Una vez en el LCR, el triptófano se convierte en serotonina en los núcleos del rafe por la vía enzimática normal. La serotonina resultante se metaboliza aún más en melatonina por la glándula pineal . Por lo tanto, estos datos sugieren que la "somnolencia inducida por el festín", o somnolencia posprandial, puede ser el resultado de una comida pesada rica en carbohidratos, que indirectamente aumenta la producción de melatonina en el cerebro y, por lo tanto, promueve el sueño.
Investigar
En 1912, Felix Ehrlich demostró que la levadura metaboliza los aminoácidos naturales esencialmente separando el dióxido de carbono y reemplazando el grupo amino por un grupo hidroxilo . Mediante esta reacción , el triptófano da lugar al triptofol .
El triptófano afecta la síntesis de serotonina en el cerebro cuando se administra por vía oral en forma purificada y se usa para modificar los niveles de serotonina para la investigación. El bajo nivel de serotonina cerebral se induce mediante la administración de proteína pobre en triptófano en una técnica llamada depleción aguda de triptófano . Los estudios que utilizan este método han evaluado el efecto de la serotonina en el estado de ánimo y el comportamiento social, encontrando que la serotonina reduce la agresión y aumenta la amabilidad.
Fluorescencia
El triptófano es una sonda fluorescente intrínseca importante (aminoácido), que se puede utilizar para estimar la naturaleza del microambiente alrededor del residuo de triptófano. La mayoría de las emisiones de fluorescencia intrínsecas de una proteína plegada se deben a la excitación de residuos de triptófano.
Ver también
- 5-hidroxitriptófano (5-HTP)
- Reacción de Acree-Rosenheim
- Reacción de Adamkiewicz
- Atenuador (genética)
- N , N- dimetiltriptamina
- Reacción Hopkins-Cole
- Serotonina
- Triptamina
Referencias
Otras lecturas
- Wood RM, Rilling JK, Sanfey AG, Bhagwagar Z, Rogers RD (mayo de 2006). "Efectos del agotamiento del triptófano en el rendimiento de un juego repetido del dilema del prisionero en adultos sanos" . Neuropsicofarmacología . 31 (5): 1075–84. doi : 10.1038 / sj.npp.1300932 . PMID 16407905 .
enlaces externos
- "KEGG PATHWAY: metabolismo del triptófano - Homo sapiens" . KEGG: Enciclopedia de genes y genomas de Kioto. 23 de agosto de 2006 . Consultado el 20 de abril de 2008 .
- GP Moss. "Catabolismo del triptófano (etapas tempranas)" . Comité de Nomenclatura de la Unión Internacional de Bioquímica y Biología Molecular (NC-IUBMB). Archivado desde el original el 13 de septiembre de 2003 . Consultado el 20 de abril de 2008 .
- GP Moss. "Catabolismo del triptófano (etapas posteriores)" . Comité de Nomenclatura de la Unión Internacional de Bioquímica y Biología Molecular (NC-IUBMB). Archivado desde el original el 13 de septiembre de 2003 . Consultado el 20 de abril de 2008 .
- B. Mikkelson; DP Mikkelson (22 de noviembre de 2007). "Turquía causa somnolencia" . Páginas de referencia de Urban Legends . Snopes.com . Consultado el 20 de abril de 2008 .