Ortoformiato de trietilo - Triethyl orthoformate
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC preferido
(Dietoximetoxi) etano |
|
| Otros nombres
Trietoximetano; Ortoformiato de etilo
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| CHEMBL | |
| ChemSpider | |
| Tarjeta de información ECHA |
100.004.138 |
| Número CE | |
|
PubChem CID
|
|
| UNII | |
| un numero | 2524 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| C 7 H 16 O 3 | |
| Masa molar | 148.202 g · mol −1 |
| Densidad | 0,891 g / ml |
| Punto de fusion | −76 ° C (−105 ° F; 197 K) |
| Punto de ebullición | 146 ° C (295 ° F; 419 K) |
| Peligros | |
| Ficha de datos de seguridad | Fischer Scientific |
| Pictogramas GHS |
 
|
| Palabra de señal GHS | Advertencia |
| H226 , H315 , H319 , H335 | |
| P210 , P233 , P240 , P241 , P242 , P243 , P261 , P264 , P271 , P280 , P302 + 352 , P303 + 361 + 353 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P370 + 378 , P403 + 233 , P403 + 235 , P405 , P501 | |
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
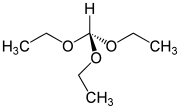
El ortoformiato de trietilo es un compuesto orgánico con la fórmula HC (OC 2 H 5 ) 3 . Este líquido volátil incoloro, el ortoéster del ácido fórmico , está disponible comercialmente. La síntesis industrial es a partir de cianuro de hidrógeno y etanol.
También se puede preparar a partir de la reacción de etóxido de sodio , formado in situ a partir de sodio y etanol absoluto , y cloroformo :
- CHCl 3 + 3 Na + 3 EtOH → HC (OEt) 3 + 3 ⁄ 2 H 2 + 3 NaCl
El ortoformiato de trietilo se utiliza en la síntesis de aldehído de Bodroux-Chichibabin , por ejemplo:
- RMgBr + HC (OC 2 H 5 ) 3 → RC (H) (OC 2 H 5 ) 2 + MgBr (OC 2 H 5 )
- RC (H) (OC 2 H 5 ) 2 + H2O → RCHO + 2 C 2 H 5 OH
En química de coordinación , se utiliza para convertir complejos metálicos aquo en los correspondientes complejos de etanol:
- [Ni (H 2 O) 6 ] (BF 4 ) 2 + 6 HC (OC 2 H 5 ) 3 → [Ni (C 2 H 5 OH) 6 ] (BF 4 ) 2 + 6 HC (O) (OC 2 H 5 ) + 6 HOC 2 H 5
El ortoformiato de trietilo (TEOF) es un reactivo excelente para convertir ácidos carboxílicos compatibles en ésteres etílicos. Dichos ácidos carboxílicos, sometidos a reflujo puro en exceso de TEOF hasta que cesa la evolución de los de bajo punto de ebullición, se convierten cuantitativamente en los ésteres etílicos, sin necesidad de catálisis extraña. Alternativamente, agregado a esterificaciones ordinarias usando ácido catalítico y etanol, TEOF ayuda a completar la esterificación al convertir el subproducto de agua formado en etanol y formiato de etilo.
Ver también
Referencias
- ^ Diccionario de productos químicos industriales de Ashford, tercera edición, 2011, página 9288
- ^ WE Kaufmann y EE Dreger (1941). "Ortoformiato de etilo" . Síntesis orgánicas . ; Volumen colectivo , 1 , p. 258
- ^ G. Bryant Bachman (1943). " n -hexaldehído" . Síntesis orgánicas . ; Volumen colectivo , 2 , p. 323
- ^ Willem L. Driessen, Jan Reedijk "Solvatos sólidos: el uso de ligandos débiles en la química de coordinación" Inorg. Synth., 1992, vol. 29,111–118. doi : 10.1002 / 9780470132609.ch27
- ^ Paine, John B. (julio de 2008). "Ésteres de ácido piromelítico. Parte I. Ésteres de alcoholes achirales: Síntesis regioselectiva de ésteres piromelitados parciales y mixtos, mecanismo de transesterificación en la esterificación cuantitativa del sistema piromelitato utilizando ésteres de ortoformiato y síntesis fácil del patrón de ortoformiato sustitutivo de diéster" . La Revista de Química Orgánica . 73 (13): 4929–4938. doi : 10.1021 / jo800543w . ISSN 0022-3263 .
