Silencer (genética) - Silencer (genetics)
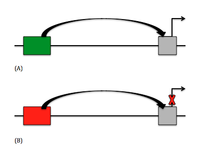
En genética , un silenciador es una secuencia de ADN capaz de unirse a factores de regulación de la transcripción , llamados represores . El ADN contiene genes y proporciona la plantilla para producir ARN mensajero (ARNm). Ese ARNm luego se traduce en proteínas. Cuando una proteína represora se une a la región silenciadora del ADN, se evita que la ARN polimerasa transcriba la secuencia de ADN en ARN. Con la transcripción bloqueada, la traducción de ARN en proteínas es imposible. Por tanto, los silenciadores evitan que los genes se expresen como proteínas.
La ARN polimerasa, una enzima dependiente del ADN, transcribe las secuencias de ADN, llamadas nucleótidos , en la dirección 3 'a 5', mientras que el ARN complementario se sintetiza en la dirección 5 'a 3'. El ARN es similar al ADN, excepto que el ARN contiene uracilo, en lugar de timina, que forma un par de bases con la adenina. Una región importante para la actividad de represión y expresión génica que se encuentra en el ARN es la región no traducida 3 ' . Ésta es una región en el extremo 3 'del ARN que no se traducirá en proteína, pero incluye muchas regiones reguladoras.
Aún no se sabe mucho sobre los silenciadores, pero los científicos continúan estudiando con la esperanza de clasificar más tipos, ubicaciones en el genoma y enfermedades asociadas con los silenciadores.
Funcionalidad
Ubicaciones dentro del genoma
Un silenciador es un elemento específico de secuencia que induce un efecto negativo en la transcripción de su gen particular. Hay muchas posiciones en las que se puede ubicar un elemento silenciador en el ADN. La posición más común se encuentra corriente arriba del gen objetivo, donde puede ayudar a reprimir la transcripción del gen. Esta distancia puede variar mucho entre aproximadamente -20 pb y -2000 pb aguas arriba de un gen. Ciertos silenciadores pueden encontrarse aguas abajo de un promotor ubicado dentro del intrón o exón del propio gen. También se han encontrado silenciadores dentro de la región no traducida de 3 primos (3 'UTR) del ARNm.
Tipos
Actualmente, existen dos tipos principales de silenciadores en el ADN, que son el elemento silenciador clásico y el elemento regulador negativo no clásico (NRE). En los silenciadores clásicos, el gen es reprimido activamente por el elemento silenciador, principalmente al interferir con el ensamblaje del factor de transcripción general (GTF). Las NRE reprimen pasivamente el gen, por lo general inhibiendo otros elementos que están aguas arriba del gen. De los NRE, hay ciertos silenciadores que dependen de la orientación, lo que significa que el factor de unión se une en una dirección particular en relación con otras secuencias. Se entiende que los silenciadores dependientes del promotor son elementos silenciadores porque son dependientes de la posición y la orientación, pero también deben utilizar un factor específico del promotor. Ha habido un descubrimiento reciente de elementos de respuesta del grupo Polycomb (PRE), que pueden permitir e inhibir la represión dependiendo de la proteína unida a ella y la presencia de transcripción no codificante.
Mecanismos
Para los silenciadores clásicos, la vía de señalización es relativamente simple. Dado que la represión es activa, los elementos silenciadores se dirigen al ensamblaje de GTF, necesarios para la transcripción del gen. Estos elementos silenciadores se encuentran en su mayoría aguas arriba del gen y pueden variar entre distancias cortas y largas. Para los silenciadores de largo alcance, se ha observado que el ADN formará un bucle para acercar el silenciador al promotor y extraer el ADN que interfiere. Los silenciadores también se dirigen a sitios de helicasa en el ADN que son ricos en adenina y timina (AT) y propensos a desenrollar el ADN, lo que deja espacio para iniciar la transcripción. La actividad helicasa inhibida conduce a la inhibición de la transcripción. Esto se ve comúnmente en el promotor del gen de tirotropina-β humana . Las NRE pueden inducir una curvatura en la región promotora para bloquear interacciones, como se ve cuando una NRE se une a Yin-Yang 1 ( YY1 ) y también a señales reguladoras de flanco o regiones promotoras. Cuando la región silenciadora se encuentra dentro de un intrón, puede haber dos tipos de represiones. Primero, puede haber un bloqueo físico de un sitio de empalme. En segundo lugar, puede haber un doblez en el ADN que inhiba el procesamiento del ARN.
Cuando se encuentra en el exón o en la región no traducida, el silenciador será principalmente clásico o dependiente de la posición. Sin embargo, estos silenciadores pueden realizar su actividad antes de la transcripción. La mayoría de los silenciadores se expresan de forma constitutiva en los organismos y solo permiten la activación de un gen inhibiendo el silenciador o activando una región potenciadora. El mejor ejemplo de esto es el factor silenciador neuronal-restrictivo (NRSF) que es producido por el gen REST . El gen REST produce NRSF para reprimir la transcripción de genes neuronales que son esenciales para la localización del tejido neuronal. Cuando un silenciador reprime REST , NRSF también se inhibe, lo que permite la transcripción de genes neuronales.
Similitudes con potenciadores
Otro elemento regulador ubicado aguas arriba del gen es un potenciador . Los potenciadores funcionan como un interruptor de "encendido" en la expresión génica y activarán la región promotora de un gen particular, mientras que los silenciadores actúan como el interruptor de "apagado". Aunque estos dos elementos reguladores trabajan uno contra el otro, ambos tipos de secuencia afectan la región promotora de formas muy similares. Debido a que los silenciadores no se han identificado y analizado a fondo, la extensa investigación sobre los potenciadores ha ayudado a los biólogos a comprender la mecánica del silenciador. Los potenciadores se pueden encontrar en muchas de las mismas áreas donde se encuentran los silenciadores, como corriente arriba del promotor por muchos pares de kilobase, o incluso corriente abajo dentro del intrón del gen. El bucle de ADN también es una función modelo utilizada por los potenciadores para acortar la proximidad del promotor al potenciador. Los potenciadores también funcionan con factores de transcripción para iniciar la expresión, al igual que los silenciadores pueden hacerlo con los represores.
En procariotas y eucariotas
Procariotas

Existen varias diferencias en la regulación del control metabólico en eucariotas y procariotas. Los procariotas varían el número de enzimas específicas producidas en sus células para regular la expresión génica, que es un control metabólico lento, y también regular las vías enzimáticas a través de mecanismos como la inhibición por retroalimentación y la regulación alostérica , que es un control metabólico rápido. Los genes de los procariotas se agrupan basándose en funciones similares en unidades llamadas operones que consisten en un promotor y un operador . El operador es el sitio de unión para el represor y por lo tanto tiene una función equivalente a la región silenciadora en el ADN eucariota. Cuando una proteína represora se une al operador, la ARN polimerasa no puede unirse al promotor para iniciar la transcripción del operón.
Represión del operón lac
El operón lac en el procariota E. coli consiste en genes que producen enzimas para descomponer la lactosa. Su operón es un ejemplo de silenciador procariota. Los tres genes funcionales de este operón son lacZ, lacY y lacA. El gen represor, lacI, producirá la proteína represora LacI que se encuentra bajo regulación alostérica. Estos genes se activan por la presencia de lactosa en la célula que actúa como molécula efectora que se une a LacI. Cuando el represor se une a la lactosa, no se unirá al operador, lo que permite que la ARN polimerasa se una al promotor para iniciar la transcripción del operón. Cuando el sitio alostérico del represor no está unido a la lactosa, su sitio activo se unirá al operador para evitar que la ARN polimerasa transcriba los genes del operón lac .
Eucariotas
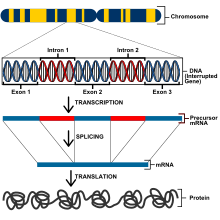
Los eucariotas tienen un genoma mucho más grande y, por lo tanto, tienen diferentes métodos de regulación génica que los procariotas. Todas las células de un organismo eucariota tienen el mismo ADN, pero se especifican a través de la expresión genética diferencial, un fenómeno conocido como totipotencia genética . Sin embargo, para que una célula exprese los genes para un funcionamiento adecuado, los genes deben estar estrechamente regulados para expresar las propiedades correctas. Los genes en eucariotas son controlados en el transcripcional , post-transcripcional , traduccional y post-traduccionales niveles. A nivel transcripcional, la expresión génica se regula alterando las tasas de transcripción. Los genes que codifican proteínas incluyen exones que codificarán los polipéptidos, intrones que se eliminan del ARNm antes de la traducción de proteínas, un sitio de inicio de la transcripción en el que se une la ARN polimerasa y un promotor.
Represión de la caja TATA
Los genes eucariotas contienen un promotor corriente arriba y un promotor central también denominado promotor basal. Un promotor basal común es la secuencia TATAAAAAA conocida como caja TATA . La caja TATA es un complejo con varias proteínas diferentes, incluido el factor de transcripción II D (TFIID), que incluye la proteína de unión a TATA (TBP) que se une a la caja TATA junto con otras 13 proteínas que se unen a TBP. Las proteínas de unión a la caja TATA también incluyen el factor de transcripción II B (TFIIB) que se une a las polimerasas de ADN y ARN.
Los silenciadores en eucariotas controlan la expresión génica en un nivel transcripcional en el que no se transcribe el ARNm. Estas secuencias de ADN pueden actuar como silenciadores o potenciadores basados en el factor de transcripción que se une a la secuencia y la unión de esta secuencia evitará que los promotores, como la caja TATA, se una a la ARN polimerasa. Una proteína represora puede tener regiones que se unen a la secuencia de ADN, así como regiones que se unen a los factores de transcripción ensamblados en el promotor del gen, lo que crearía un mecanismo de bucle cromosómico. El bucle acerca a los silenciadores a los promotores para garantizar que los grupos de proteínas necesarios para la expresión génica óptima trabajen juntos.
Silenciadores mutados, enfermedades hereditarias y sus efectos
Las mutaciones genéticas ocurren cuando se alteran las secuencias de nucleótidos en un organismo. Estas mutaciones conducen no solo a influencias fenotípicas observables en un individuo, sino también a alteraciones que son fenotípicamente indetectables. Las fuentes de estas mutaciones pueden ser errores durante la replicación, mutaciones espontáneas y mutágenos químicos y físicos ( radiación ultravioleta y ionizante , calor). Los silenciadores, al estar codificados en el genoma, son susceptibles a tales alteraciones que, en muchos casos, pueden conducir a graves anomalías fenotípicas y funcionales. En términos generales, las mutaciones en los elementos o regiones silenciadores podrían conducir a la inhibición de la acción del silenciador oa la represión persistente de un gen necesario. Esto puede conducir entonces a la expresión o supresión de un fenotipo no deseado que puede afectar la funcionalidad normal de ciertos sistemas en el organismo. Entre los muchos elementos y proteínas silenciadores, REST / NSRF es un factor silenciador importante que tiene una variedad de impactos, no solo en los aspectos neuronales del desarrollo. De hecho, en muchos casos, REST / NSRF actúa junto con RE-1 / NRSE para reprimir e influir en las células no neuronales. Sus efectos van desde las ranas ( Xenopus laevis ) hasta los humanos, con innumerables efectos en el fenotipo y también en el desarrollo. En Xenopus laevis , el mal funcionamiento o daño de REST / NRSF se ha asociado con un patrón ectodérmico anormal durante el desarrollo y consecuencias significativas en el tubo neural, los ganglios craneales y el desarrollo del ojo. En humanos, una deficiencia en el elemento silenciador REST / NSRF se ha correlacionado con la enfermedad de Huntington debido a la disminución en la transcripción de BDNF .
Además, los estudios en curso indican que NRSE está involucrado en la regulación del gen ANP, que cuando se sobreexpresa, puede conducir a hipertrofia ventricular . Las mutaciones en los complejos del grupo Polycomb (PcG) también presentaron modificaciones significativas en los sistemas fisiológicos de los organismos. Por lo tanto, la modificación de los elementos y secuencias del silenciador puede resultar en cambios devastadores o imperceptibles.
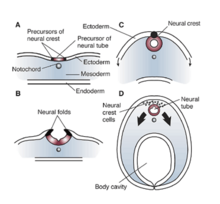
REST / NRSF en Xenopus laevis
Los efectos e influencias de RE1 / NRSE y REST / NRSF son significativos en células no neuronales que requieren la represión o silenciamiento de genes neuronales. Estos elementos silenciadores también regulan la expresión de genes que no inducen proteínas específicas de neuronas y los estudios han demostrado el gran impacto que estos factores tienen en los procesos celulares. En Xenopus laevis, la disfunción o mutación RE1 / NRSE y REST / NRSF demostraron un impacto significativo en el desarrollo del tubo neural , los ganglios craneales y el ojo. Todas estas alteraciones pueden atribuirse a un patrón inadecuado del ectodermo durante el desarrollo de Xenopus. Por tanto, una mutación o alteración en la región de silenciamiento RE1 / NRSE o el factor silenciador REST / NRSF puede interrumpir la diferenciación y especificación adecuadas del dominio neuroepitelial y también obstaculizar la formación de piel o ectodermo. La falta de estos factores resulta en una disminución de la producción de proteína morfogenética ósea (BMP), lo que se traduce en un desarrollo deficiente de la cresta neural . Por lo tanto, los efectos de NRSE y NRSF son de fundamental importancia para la neurogénesis del embrión en desarrollo y también en las primeras etapas del patrón ectodérmico. En última instancia, el funcionamiento inadecuado de estos factores puede resultar en un tubo neural aberrante, ganglios craneales y desarrollo ocular en Xenopus .
REST / NSRF y enfermedad de Huntington
La enfermedad de Huntington (EH) es un trastorno neurodegenerativo hereditario, con síntomas que surgen durante la edad adulta media del individuo. Los síntomas más notorios de esta enfermedad progresiva son las alteraciones cognitivas y motoras, así como las alteraciones del comportamiento. Estos impedimentos pueden convertirse en demencia , corea y eventualmente la muerte. A nivel molecular, la EH es el resultado de una mutación en la proteína huntingtina (Htt). Más específicamente, hay una repetición anormal de una secuencia CAG hacia el extremo 5 'del gen, que luego conduce al desarrollo de un tramo de poliglutamina tóxico (polyQ) en la proteína. La proteína Htt mutada afecta las funciones neuronales adecuadas de un individuo al inhibir la acción de REST / NRSF.
REST / NRSF es un importante elemento silenciador que se une a regiones reguladoras para controlar la expresión de ciertas proteínas involucradas en funciones neurales. Las acciones mecánicas de la huntingtina aún no se comprenden completamente, pero existe una correlación entre Htt y REST / NRSF en el desarrollo de la EH. Al unirse al REST / NRSF, la proteína huntingtina mutada inhibe la acción del elemento silenciador y lo retiene en el citosol. Por tanto, REST / NRSF no puede entrar en el núcleo y unirse al elemento regulador RE-1 / NRSE de 21 pares de bases. Una represión adecuada de genes diana específicos es de fundamental importancia, ya que muchos están involucrados en el correcto desarrollo de receptores neuronales, neurotransmisores , proteínas de vesículas sinápticas y proteínas de canal. Una deficiencia en el desarrollo adecuado de estas proteínas puede causar las disfunciones neurales que se observan en la enfermedad de Huntington. Además de la falta de represión debida al REST / NRSF inactivo, la proteína huntingtina mutada también puede disminuir la transcripción del gen del factor neurotrópico derivado del cerebro (BDNF). El BDNF influye en la supervivencia y el desarrollo de las neuronas del sistema nervioso central y del sistema nervioso periférico. Esta represión anormal ocurre cuando la región RE1 / NRSE dentro de la región promotora BDNF es activada por la unión de REST / NRSF, lo que conduce a la falta de transcripción del gen BDNF. Por tanto, la represión anómala de la proteína BDNF sugiere un impacto significativo en la enfermedad de Huntington.
Investigación actual sobre REST / NRSF e hipertrofia ventricular en mamíferos
REST / NRSF junto con RE1 / NRSE también actúa fuera del sistema nervioso como reguladores y represores. La investigación actual ha relacionado la actividad RE1 / NRSE con la regulación de la expresión del gen del péptido natriurético auricular ( ANP ). Una región reguladora NRSE está presente en la región no traducida 3 'del gen ANP y actúa como mediador para su expresión apropiada. La proteína codificada por el gen ANP es importante durante el desarrollo embrionario para la maduración y desarrollo de los miocitos cardíacos . Sin embargo, durante la primera infancia y durante la edad adulta, la expresión de ANP se suprime o se mantiene al mínimo en el ventrículo. Por lo tanto, una inducción anormal del gen ANP puede provocar hipertrofia ventricular y consecuencias cardíacas graves. Para mantener la represión del gen, NRSF (factor silenciador restrictivo de neuronas) o REST se une a la región NRSE en la región 3 'no traducida del gen ANP . Además, el complejo NRSF-NRSE recluta un correpresor transcripcional conocido como mSin3. Esto conduce a la actividad de la histona desacetilasa en la región y a la represión del gen. Por lo tanto, los estudios han revelado la correlación entre REST / NRSF y RE1 / NRSE en la regulación de la expresión del gen ANP en miocitos ventriculares. Una mutación en NRSF o NRSE puede conducir a un desarrollo indeseable de miocitos ventriculares, debido a la falta de represión, que luego puede causar hipertrofia ventricular. La hipertrofia ventricular izquierda, por ejemplo, aumenta la posibilidad de muerte súbita de un individuo debido a una arritmia ventricular resultante del aumento de la masa ventricular. Además de la influencia sobre el gen ANP , la secuencia NRSE regula otros genes embrionarios cardíacos, como el péptido natriurético cerebral BNP, la α-actina esquelética y la subunidad α3 de Na, K-ATPasa. Por tanto, la actividad reguladora tanto de NRSE como de NRSF en mamíferos previene no solo disfunciones neurales sino también anomalías fisiológicas y fenotípicas en otras regiones no neuronales del cuerpo.
Mutaciones en los elementos de respuesta del grupo polycomb (PRE)
Los complejos reguladores del grupo Polycomb (PcG) son conocidos por su influencia en la regulación epigenética de las células madre, específicamente en las células madre hematopoyéticas . El Polycomb Repressive Complex 1 (PRC 1) está directamente involucrado en el proceso de hematopoyesis y funciona junto con, por ejemplo, el gen PcG “ Bmi1 ”. Los estudios en ratones indican que los organismos con "Bmi1" mutado demuestran un funcionamiento mitocondrial deficiente y también obstaculizan la capacidad de las células hematopoyéticas para autorrenovarse. Asimismo, las mutaciones en los genes PRC2 se relacionaron con afecciones hematológicas como la leucemia linfoblástica aguda (LLA), que es una forma de leucemia. Por lo tanto, los genes y proteínas del grupo Polycomb están involucrados en el mantenimiento adecuado de la hematopoyesis en el cuerpo.
Referencias
enlaces externos
- Silencer + Elements en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .