Cloruro de nitrosilo - Nitrosyl chloride
|
|

|
|
| Nombres | |
|---|---|
|
Nombre IUPAC
Cloruro de nitrosilo
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| Tarjeta de información ECHA |
100.018.430 |
| Número CE | |
| Número e | E919 (agentes de glaseado, ...) |
| Malla | nitrosilo + cloruro |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| un numero | 1069 |
|
Tablero CompTox ( EPA )
|
|
|
|
|
|
| Propiedades | |
| NOCl | |
| Masa molar | 65,459 g mol −1 |
| Apariencia | Gas amarillo |
| Densidad | 2.872 mg mL −1 |
| Punto de fusion | −59,4 ° C (−74,9 ° F; 213,8 K) |
| Punto de ebullición | −5,55 ° C (22,01 ° F; 267,60 K) |
| Reacciona | |
| Estructura | |
| Diedro, digonal | |
| Hibridación | sp 2 en N |
| 1,90 D | |
| Termoquímica | |
|
Entropía molar estándar ( S |
261,68 JK −1 mol −1 |
| 51,71 kJ mol −1 | |
| Riesgos | |
| Ficha de datos de seguridad | inchem.org |
| NFPA 704 (diamante de fuego) | |
| Compuestos relacionados | |
|
Compuestos relacionados
|
|
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencias de Infobox | |
El cloruro de nitrosilo es el compuesto químico con la fórmula NOCl. Es un gas amarillo que se encuentra comúnmente como componente del agua regia , una mezcla de 3 partes de ácido clorhídrico concentrado y 1 parte de ácido nítrico concentrado . Es un fuerte electrófilo y agente oxidante . A veces se le llama reactivo de Tilden.
Estructura y síntesis
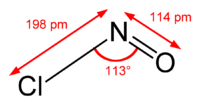
La molécula está doblada. Existe un enlace doble entre N y O (distancia = 1,16 Å) y un enlace sencillo entre N y Cl (distancia = 1,96 Å). El ángulo O = N – Cl es 113 °.
Producción
El cloruro de nitrosilo se puede producir de muchas formas.
- La combinación de ácido nitrosilsulfúrico y HCl proporciona el compuesto. Este método se utiliza industrialmente.
- HCl + NOHSO 4 → H 2 SO 4 + NOCl
- Un método de laboratorio más conveniente implica la deshidratación (reversible) del ácido nitroso por HCl
- HNO 2 + HCl → H 2 O + NOCl
- Por la combinación directa de cloro y óxido nítrico ; Esta reacción se invierte por encima de los 100 ° C.
- Cl 2 + 2 NO → 2 NOCl
- Por reducción de dióxido de nitrógeno con cloruro de hidrógeno:
- 2NO 2 + 4 HCl → 2NOCl + 2H 2 O + Cl 2
Ocurrencia en aqua regia
El NOCl también surge de la combinación de ácidos clorhídrico y nítrico de acuerdo con la siguiente reacción:
- HNO 3 + 3 HCl → 2 [Cl] + 2 H 2 O + NOCl
En el ácido nítrico, el NOCl se oxida fácilmente en dióxido de nitrógeno . La presencia de NOCl en agua regia fue descrita por Edmund Davy en 1831.
Reacciones
El NOCl se comporta como electrófilo y oxidante en la mayoría de sus reacciones. Con aceptores de haluros , por ejemplo pentacloruro de antimonio , se convierte en sales de nitrosonio :
- NOCl + SbCl 5 → [NO] + [SbCl 6 ] -
En una reacción relacionada, el ácido sulfúrico da ácido nitrosilsulfúrico , el anhídrido de ácido mixto de ácido nitroso y sulfúrico:
- ClNO + H 2 SO 4 → ONHSO 4 + HCl
El NOCl reacciona con el tiocianato de plata para dar cloruro de plata y el pseudohalógeno tiocianato de nitrosilo:
- ClNO + AgSCN → AgCl + ONSCN
De manera similar, reacciona con el cianuro de plata para dar cianuro de nitrosilo .
El cloruro de nitrosilo se utiliza para preparar complejos metálicos de nitrosilo . Con hexacarbonilo de molibdeno , NOCl da el complejo de dinitrosildicloruro:
- Mo (CO) 6 + 2 NOCl → MoCl 2 (NO) 2 + 6 CO
Disuelve el platino:
- Pt + 6 NOCl → (NO + ) 2 [PtCl 6 ] 2- + 4 NO
Aplicaciones en síntesis orgánica
Aparte de su papel en la producción de caprolactama, el NOCl encuentra otros usos en la síntesis orgánica . Se agrega a los alquenos para producir α- clorooximas . La adición de NOCl sigue la regla de Markovnikov . Los cetenos también agregan NOCl, dando derivados de nitrosilo:
- H 2 C = C = O + NOCl → ONCH 2 C (O) Cl
Los epóxidos reaccionan con NOCl para dar derivados de α-cloronitritoalquilo. En el caso del óxido de propileno, la adición procede con alta regioquímica:
Convierte amidas en derivados N- nitroso. El NOCl convierte algunas aminas cíclicas en alquenos. Por ejemplo, la aziridina reacciona con NOCl para dar eteno , óxido nitroso y cloruro de hidrógeno .
Aplicaciones industriales
El NOCl y el ciclohexano reaccionan fotoquímicamente para dar hidrocloruro de ciclohexanona oxima . Este proceso aprovecha la tendencia del NOCl a experimentar fotodisociación en radicales NO y Cl. El óxido se convierte en caprolactama , un precursor del Nylon-6 .
La seguridad
El cloruro de nitrosilo es muy tóxico e irrita los pulmones, los ojos y la piel.
Referencias
enlaces externos
-
 Medios relacionados con el cloruro de nitrosilo en Wikimedia Commons
Medios relacionados con el cloruro de nitrosilo en Wikimedia Commons


