GSK-3 - GSK-3
| Glucógeno sintasa quinasa 3, dominio catalítico | |
|---|---|
| Identificadores | |
| Símbolo | STKc_GSK3 |
| InterPro | IPR039192 |
| CDD | cd14137 |
| glucógeno sintasa quinasa 3 alfa | |||||||
|---|---|---|---|---|---|---|---|
| Identificadores | |||||||
| Símbolo | GSK3A | ||||||
| Gen NCBI | 2931 | ||||||
| HGNC | 4616 | ||||||
| OMIM | 606784 | ||||||
| RefSeq | NM_019884 | ||||||
| UniProt | P49840 | ||||||
| Otros datos | |||||||
| Número CE | 2.7.11.26 | ||||||
| Lugar | Chr. 19 q13.2 | ||||||
| |||||||
| glucógeno sintasa quinasa 3 beta | |||||||
|---|---|---|---|---|---|---|---|
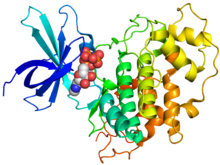
Estructura cristalográfica de GSK-3β humana (color del arco iris, N-terminal = azul, C-terminal = rojo) unida al éster de adenilato de ácido fosfoaminofosfónico (esferas).
| |||||||
| Identificadores | |||||||
| Símbolo | GSK3B | ||||||
| Gen NCBI | 2932 | ||||||
| HGNC | 4617 | ||||||
| OMIM | 605004 | ||||||
| PDB | 1T3W Más estructuras | ||||||
| RefSeq | NM_002093 | ||||||
| UniProt | P49841 | ||||||
| Otros datos | |||||||
| Número CE | 2.7.11.26 | ||||||
| Lugar | Chr. 3 q13.33 | ||||||
| |||||||
La glucógeno sintasa quinasa 3 ( GSK-3 ) es una proteína quinasa de serina / treonina que media la adición de moléculas de fosfato a los residuos de aminoácidos de serina y treonina . Descubierta por primera vez en 1980 como una quinasa reguladora de su homónimo, la glucógeno sintasa (GS), la GSK-3 se ha identificado desde entonces como una proteína quinasa para más de 100 proteínas diferentes en una variedad de vías diferentes. En los mamíferos, incluidos los humanos, GSK-3 existe en dos isoformas codificadas por dos genes parálogos GSK-3α ( GSK3A ) y GSK-3β ( GSK3B ). GSK-3 ha sido objeto de mucha investigación ya que se ha relacionado con una serie de enfermedades, incluida la diabetes tipo 2 , la enfermedad de Alzheimer , la inflamación , el cáncer y el trastorno bipolar .
GSK-3 es una proteína quinasa de serina / treonina que fosforila la treonina o la serina , y esta fosforilación controla una variedad de actividades biológicas, como el metabolismo del glucógeno , la señalización celular , el transporte celular y otras. La inhibición de GS por GSK-3β conduce a una disminución de la síntesis de glucógeno en el hígado y los músculos, junto con un aumento de la glucosa en sangre o hiperglucemia. Esta es la razón por la que GSK-3β se asocia con la patogénesis y la progresión de muchas enfermedades, como la diabetes , la obesidad , el cáncer y la enfermedad de Alzheimer. Es activo en las células en reposo y es inhibido por varias hormonas como la insulina , el factor de crecimiento endotelial y el factor de crecimiento derivado de las plaquetas . La insulina la inactiva por fosforilación de los residuos de serina específicos Ser21 y Ser9 en las isoformas α y β de GSK-3, respectivamente. De forma dependiente de fosfatidilinositol 3-quinasa.
A partir de 2019, GSK-3 es el único tipo de glucógeno sintasa quinasa nombrado y reconocido. Los símbolos genéticos para GSK1 y GSK2 han sido retirados por el Comité de Nomenclatura Genética de HUGO (HGNC) y no se han especificado nuevos nombres para estos "genes" ni sus ubicaciones.
Mecanismo
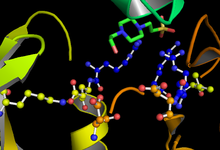
GSK-3 funciona fosforilando un residuo de serina o treonina en su sustrato objetivo. Un bolsillo cargado positivamente adyacente al sitio activo se une a un grupo fosfato "cebador" unido a una serina o treonina de cuatro residuos C-terminal del sitio de fosforilación diana. El sitio activo, en los residuos 181, 200, 97 y 85, se une al fosfato terminal de ATP y lo transfiere a la ubicación objetivo en el sustrato (ver figura 1).
Glucógeno sintasa
La glucógeno sintasa es una enzima responsable de la síntesis de glucógeno . Es activado por glucosa 6-fosfato (G6P) e inhibido por glucógeno sintasa quinasas ( GSK3 ). Estos dos mecanismos juegan un papel importante en el metabolismo del glucógeno.
Función
La fosforilación de una proteína por GSK-3 normalmente inhibe la actividad de su objetivo aguas abajo. GSK-3 es activo en una serie de vías de señalización intracelular centrales, incluida la proliferación celular, la migración, la regulación de la glucosa y la apoptosis.
GSK-3 se descubrió originalmente en el contexto de su participación en la regulación de la glucógeno sintasa . Después de ser cebado por caseína quinasa 2 (CK2), la glucógeno sintasa se fosforila en un grupo de tres residuos de serina C-terminal, reduciendo su actividad. Además de su papel en la regulación de la glucógeno sintasa, GSK-3 se ha implicado en otros aspectos de la homeostasis de la glucosa, incluida la fosforilación del receptor de insulina IRS1 y de las enzimas gluconeogénicas fosfoenolpiruvato carboxiquinasa y glucosa 6 fosfatasa . Sin embargo, estas interacciones no se han confirmado, ya que estas vías pueden inhibirse sin la regulación positiva de GSK-3.
También se ha demostrado que GSK-3 regula los procesos inmunes y migratorios. GSK-3 participa en una serie de vías de señalización en la respuesta inmune innata, incluida la producción de citocinas proinflamatorias e interleucinas. La inactivación de GSK3B por diversas proteína quinasas también afecta la respuesta inmune adaptativa al inducir la producción y proliferación de citocinas en células T CD4 + vírgenes y de memoria. En la migración celular, un aspecto integral de las respuestas inflamatorias, se ha informado que la inhibición de GSK-3 juega roles conflictivos, ya que se ha demostrado que la inhibición local en los conos de crecimiento promueve la motilidad mientras que la inhibición global de GSK-3 celular inhibe propagación y migración celular.
GSK-3 también está integralmente ligado a las vías de proliferación celular y apoptosis. Se ha demostrado que GSK-3 fosforila la beta-catenina , por lo que se dirige a la degradación. Por lo tanto, GSK-3 es parte de la vía canónica Beta-catenina / Wnt , que indica a la célula que se divida y prolifere. GSK-3 también participa en una serie de vías de señalización apoptóticas mediante la fosforilación de factores de transcripción que regulan la apoptosis . GSK-3 puede promover la apoptosis activando factores proapoptóticos como p53 e inactivando los factores promotores de la supervivencia a través de la fosforilación. Sin embargo, el papel de GSK-3 en la regulación de la apoptosis es controvertido, ya que algunos estudios han demostrado que los ratones knockout de GSK-3β están demasiado sensibilizados a la apoptosis y mueren en la etapa embrionaria, mientras que otros han demostrado que la sobreexpresión de GSK-3 puede inducir la apoptosis. . En general, GSK-3 parece promover e inhibir la apoptosis, y esta regulación varía según el contexto celular y molecular específico.
Regulación
Debido a su importancia en numerosas funciones celulares, la actividad de GSK-3 está sujeta a una estricta regulación.
La velocidad y la eficacia de la fosforilación de GSK-3 están reguladas por varios factores. La fosforilación de ciertos residuos de GSK-3 puede aumentar o disminuir su capacidad para unirse al sustrato. La fosforilación en tirosina-216 en GSK-3β o tirosina-279 en GSK-3α mejora la actividad enzimática de GSK-3, mientras que la fosforilación de serina-9 en GSK-3β o serina-21 en GSK-3α disminuye significativamente la disponibilidad del sitio activo ( ver figura 1). Además, GSK-3 es inusual entre las quinasas porque normalmente requiere una "quinasa de cebado" para fosforilar primero un sustrato. Un residuo de serina o treonina fosforilado situado en el extremo C de cuatro aminoácidos del sitio diana de fosforilación permite que el sustrato se una a una bolsa de carga positiva formada por residuos de arginina y lisina.
Dependiendo de la vía en la que se utilice, GSK-3 puede regularse adicionalmente mediante la localización celular o la formación de complejos de proteínas. La actividad de GSK-3 es mucho mayor en el núcleo y las mitocondrias que en el citosol en las neuronas corticales, mientras que la fosforilación de Beta-catenina por GSK-3 está mediada por la unión de ambas proteínas a Axin , una proteína de andamio, lo que permite que Beta -catenina para acceder al sitio activo de GSK-3.
Relevancia de la enfermedad
Debido a su participación en un gran número de vías de señalización, GSK-3 se ha asociado con una serie de enfermedades de alto perfil. Los inhibidores de GSK-3 se están probando actualmente para determinar sus efectos terapéuticos en la enfermedad de Alzheimer , la diabetes mellitus tipo 2 (DM2), algunas formas de cáncer y el trastorno bipolar .
Ahora se ha demostrado que el litio , que se utiliza como tratamiento para el trastorno bipolar , actúa como estabilizador del estado de ánimo al inhibir selectivamente GSK-3. Se desconoce el mecanismo a través del cual la inhibición de GSK-3 estabiliza el estado de ánimo, aunque se sospecha que la inhibición de la capacidad de GSK-3 para promover la inflamación contribuye al efecto terapéutico. La inhibición de GSK-3 también desestabiliza el represor transcripcional alfa Rev-ErbA, que tiene un papel importante en el reloj circadiano. Los elementos del reloj circadiano pueden estar relacionados con la predisposición al trastorno bipolar del estado de ánimo.
La actividad de GSK-3 se ha asociado con ambas características patológicas de la enfermedad de Alzheimer, a saber, la acumulación de depósitos de amiloide-β (Aβ) y la formación de ovillos neurofibrilares . Se cree que GSK-3 promueve directamente la producción de Aβ y está ligada al proceso de hiperfosforilación de las proteínas tau , lo que conduce a los ovillos. Debido a estas funciones de GSK-3 en la promoción de la enfermedad de Alzheimer, los inhibidores de GSK-3 pueden tener efectos terapéuticos positivos en los pacientes de Alzheimer y actualmente se encuentran en las primeras etapas de prueba.
De manera similar, la inhibición dirigida de GSK-3 puede tener efectos terapéuticos sobre ciertos tipos de cáncer. Aunque se ha demostrado que GSK-3 promueve la apoptosis en algunos casos, también se ha informado que es un factor clave en la tumorigénesis en algunos cánceres. En apoyo de esta afirmación, se ha demostrado que los inhibidores de GSK-3 inducen la apoptosis en células de glioma y cáncer de páncreas.
Los inhibidores de GSK-3 también se han mostrado prometedores en el tratamiento de la DM2. Aunque la actividad de GSK-3 en condiciones de diabetes puede diferir radicalmente entre diferentes tipos de tejidos, los estudios han demostrado que la introducción de inhibidores competitivos de GSK-3 puede aumentar la tolerancia a la glucosa en ratones diabéticos. Los inhibidores de GSK-3 también pueden tener efectos terapéuticos sobre la transformación hemorrágica después de un accidente cerebrovascular isquémico agudo. GSK-3 puede regular negativamente la vía de señalización de la insulina inhibiendo IRS1 a través de la fosforilación de la serina-332, haciendo que el receptor de insulina sea incapaz de activar IRS1 e iniciando aún más la vía canónica PI3K / Akt. El papel que podría desempeñar la inhibición de GSK-3 en sus otros roles de señalización aún no se comprende del todo.
La inhibición de GSK-3 también media un aumento en la transcripción del factor de transcripción Tbet (Tbx21) y una inhibición de la transcripción del co-receptor inhibidor de muerte celular programada-1 (PD-1) en las células T. Los inhibidores de GSK-3 aumentaron la función CTL CD8 (+) OT-I in vivo y la eliminación de infecciones virales por gamma-herpesvirus 68 murino y el clon 13 de coriomeningitis linfocítica, así como anti-PD-1 en inmunoterapia.
Inhibidores
Los inhibidores de la glucógeno sintasa quinasa son diferentes quimiotipos y tienen mecanismos de acción variables; pueden ser cationes , de fuentes naturales, inhibidores competitivos de ATP y no ATP sintéticos e inhibidores competitivos de sustrato. GSK3 es una arquitectura bi-lobar con N-terminal y C-terminal , el N-terminal es responsable de la unión de ATP y el C-terminal que se llama como bucle de activación media la actividad de la quinasa, la tirosina ubicada en el C-terminal es esencial para actividad completa de GSK3.
Beneficios de los inhibidores de GSK-3β
En la diabetes, los inhibidores de GSK-3β aumentan la sensibilidad a la insulina, la síntesis de glucógeno y el metabolismo de la glucosa en los músculos esqueléticos y reducen la obesidad al afectar el proceso de adipogénesis . GSK-3β también se sobreexpresa en varios tipos de cánceres, como el cáncer colorrectal , de ovario y de próstata . Los inhibidores de GSK-3β también ayudan en el tratamiento de la enfermedad de Alzheimer , los accidentes cerebrovasculares y los trastornos del estado de ánimo , incluido el trastorno bipolar .
Agentes específicos
Los inhibidores de GSK-3 incluyen:
Cationes metálicos
ATP-competitivo
Derivado de organismos marinos
- 6-BIO (IC 50 = 1,5 μM)
- Dibromocantharelline (IC 50 = 3μM)
- Himenialdesina (IC 50 = 10 nM)
- Indirrubina (IC 50 = 5-50nM)
- Meridianin
Aminopirimidinas
Arilindolmaleimida
Tiazoles
- AR-A014418 (IC 50 = 104 nm)
- AZD-1080
Paullones
IC 50 = 4-80nM:
Aloisinas
IC 50 = 0,5-1,5 μM:
No competitivo ATP
Derivado de organismos marinos
- Manzamina A (IC 50 = 1,5 μM)
- Palinurina (IC 50 = 4,5 μM)
- Tricantina (IC 50 = 7,5 μM)
Tiazolidinedionas
- TDZD-8 (IC 50 = 2 μM)
- NP00111 (IC 50 = 2 μM)
- NP031115 (IC 50 = 4 μM)
- Tideglusib
Halometilcetonas
- HMK-32 (IC 50 = 1,5 μM)
Péptidos
Mecanismo desconocido (inhibidores de moléculas pequeñas)
Litio
El litio, que se utiliza en el tratamiento del trastorno bipolar, fue el primer inhibidor natural de GSK-3 descubierto. Inhibe GSK-3 directamente por competencia con iones magnesio e indirectamente por fosforilación y autorregulación de serina. Se ha descubierto que el litio tiene efectos similares a los de la insulina sobre el metabolismo de la glucosa, incluida la estimulación de la síntesis de glucógeno en las células grasas, la piel y los músculos, aumentando la captación de glucosa y la activación de la actividad de GS. Además de la inhibición de GSK-3, también inhibe otras enzimas implicadas en la regulación del metabolismo de la glucosa, como la mioinositol-1-monofosfatasa y la 1,6 bisfosfatasa. Además, ha mostrado beneficio terapéutico en el Alzheimer y otras enfermedades neurodegenerativas como la neurodegeneración epiléptica.
Naproxeno y Cromolyn
El naproxeno es un fármaco antiinflamatorio no esteroideo, mientras que el cromolín es un agente antialérgico que actúa como estabilizador de mastocitos . Ambos fármacos han demostrado el efecto anticanceroso además del efecto hipoglucemiante debido a la inhibición de la glucógeno sintasa quinasa-3β (GSK-3β).
Para validar la hipótesis anti-GSK-3β de naproxeno y cromolín, se realizó el acoplamiento de las dos estructuras contra el bolsillo de unión de GSK-3β y se comparó su ajuste con el conocido inhibidor de GSK-3β ARA014418, además de medir la glucosa sérica, insulina sérica, péptido C sérico, variación de peso y niveles de glucógeno hepático para modelos de animales en ayunas normales y diabéticos para evaluar sus efectos hipoglucémicos in vitro.
El naproxeno y el cromolín se acoplaron con éxito en el sitio de unión de GSK-3β (ambos se colocaron en su bolsillo de unión). Exhibieron interacciones electrostáticas, hidrófobas y de enlace de hidrógeno con aminoácidos clave dentro del bolsillo de unión con perfiles de interacción de unión similares a AR-A014418 (el inhibidor conocido). Las cargas negativas de los grupos de ácido carboxílico en ambos fármacos interactúan electrostáticamente con el grupo de guanidina cargado positivamente de Arg141. Además, las interacciones de enlace de hidrógeno entre restos de ácido carboxílico de cromoglicano y los grupos amonio de Lys183 y Lys60, además del apilamiento π del sistema de anillo de naftaleno de naproxeno con el anillo fenólico de Tyr134.
Efectos antidiabéticos del naproxeno y el cromolín: en modelos animales normales, ambos fármacos han mostrado una reducción dependiente de la dosis en los niveles de glucosa en sangre y un aumento en los niveles de glucógeno. En el modelo de diabetes tipo II crónica, los niveles de glucosa también se redujeron y el nivel de glucógeno y los niveles de insulina se elevaron de una manera dependiente de la dosis con una reducción de la glucosa plasmática.
Efectos contra la obesidad del naproxeno y el cromoglicato: Ambos fármacos mostraron efectos contra la obesidad significativos, ya que reducen el peso corporal, la resistina y los niveles de glucosa de una manera dependiente de la dosis. También se encontró que elevaban los niveles de adiponectina , insulina y péptido C de una manera dependiente de la dosis.
Famotidina
La famotidina es un antagonista H2 específico de acción prolongada que disminuye la secreción de ácido gástrico. Se utiliza en el tratamiento de la úlcera péptica, la ERGE y las afecciones hipersecretoras patológicas, como el síndrome de Zollinger-Ellison. (14,15) Los antagonistas del receptor H2 afectan el metabolismo hormonal, pero su efecto sobre el metabolismo de la glucosa no está bien establecido. (16) Un estudio ha revelado un efecto hipoglucemiante de la famotidina. Recientemente, se realizó un acoplamiento molecular como prueba preliminar de detección in-silico para estudiar la unión de famotidina al sitio activo de GSK-3β.
El estudio de la unión de famotidina a la enzima ha demostrado que la famotidina se puede acoplar dentro del bolsillo de unión de GSK-3β haciendo interacciones significativas con puntos clave dentro del bolsillo de unión de GSK-3β. Las interacciones fuertes del enlace de hidrógeno con los aminoácidos clave PRO-136 y VAL -135 y la posible interacción hidrófoba con LEU-188 fueron similares a las encontradas en la unión del ligando a la enzima (AR-A014418).
Además, la famotidina mostró una alta afinidad de unión a GSK-3β y actividad inhibidora debido a las interacciones que estabilizan el complejo, a saber, el enlace de hidrógeno del grupo guanidina en la famotidina con el resto sulfahidrilo en CYS-199; e interacciones electrostáticas entre el mismo grupo guanidina con el grupo carboxilo en ASP-200, el enlace de hidrógeno entre el grupo NH2 terminal, el OH del TYR-143, y la interacción hidrófoba del átomo de azufre en el tioéter con ILE-62. Los estudios in vitro mostraron que la famotidina inhibe la actividad de GSK-3β y aumenta las reservas de glucógeno hepático de una manera dependiente de la dosis. Se observó un aumento de cuatro veces en el nivel de glucógeno hepático con el uso de la dosis más alta de famotidina (4,4 mg / kg). Además, se ha demostrado que la famotidina disminuye los niveles de glucosa sérica 30 y 60 minutos después de la carga de glucosa oral en individuos sanos.
Curcumina
La curcumina, que es un componente de la especia de cúrcuma , tiene propiedades aromatizantes y colorantes. Tiene dos formas simétricas: enol (las formas más abundantes) y cetona.
La curcumina tiene una amplia actividad farmacológica: efectos antiinflamatorios, antimicrobianos, hipoglucémicos, antioxidantes y cicatrizantes. En modelos animales con enfermedad de Alzheimer, tiene efecto anti-destructivo de beta amiloide en el cerebro, y recientemente muestra actividad anti-palúdica.
La curcumina también tiene efectos quimiopreventivos y anticancerígenos, y se ha demostrado que atenúa el estrés oxidativo y la disfunción renal en animales diabéticos con uso crónico.
El mecanismo de acción de la curcumina es antiinflamatorio; inhibe el activador transcripcional nuclear kappa B ( NF-KB ) que se activa siempre que hay respuesta inflamatoria.
NF-kB tiene dos factores reguladores, IkB y GSK-3, lo que sugiere que la curcumina se une e inhibe directamente a GSK-3B. Un estudio in vitro confirmó la inhibición de GSK-3B mediante la simulación del acoplamiento molecular mediante una técnica de acoplamiento silico. La concentración a la que la curcumina inhibiría el 50% de GK-3B es 66,3 nM.
Entre sus dos formas, los estudios experimentales y teóricos muestran que la forma enol es la forma preferida debido a su enlace de hidrógeno intramolecular, y un experimento de RMN muestra que la forma enol existe en una variedad de disolventes.
Olanzapina
Los medicamentos antipsicóticos se usan cada vez más para la esquizofrenia , el trastorno bipolar, la ansiedad y otras afecciones psiquiátricas Los antipsicóticos atípicos se usan con más frecuencia que los antipsicóticos de primera generación porque disminuyen el riesgo de síntomas extrapiramidales, como discinesia tardía , y tienen una mejor eficacia.
La olanzapina y los antipsicóticos atípicos inducen el aumento de peso al aumentar la grasa corporal. También afecta el metabolismo de la glucosa y varios estudios muestran que puede empeorar la diabetes.
Un estudio reciente muestra que la olanzapina inhibe la actividad de GSK3, lo que sugiere que la olanzapina permite la síntesis de glucógeno. Un estudio del efecto de la olanzapina en los niveles de glucógeno y glucógeno en sangre de ratón mostró una disminución significativa en el nivel de glucosa en sangre y una elevación del nivel de glucógeno en ratones, y el IC50% de olanzapina fue de 91,0 nm, que se considera un inhibidor potente. El estudio también ilustra que el uso subcrónico de olanzapina produce una potente inhibición de GSK3.
Derivados de pirimidina
Los análogos de pirimidina son antimetabolitos que interfieren con la síntesis de ácidos nucleicos. Se ha demostrado que algunos de ellos se ajustan al bolsillo de unión de ATP de GSK-3β para reducir los niveles de glucosa en sangre y mejorar algunas enfermedades neuronales.
Ver también
Referencias
enlaces externos
- Glucógeno sintasa quinasa 3 en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .