Dicloruro de disulfuro - Disulfur dichloride
|
|||
|
|
|||
| Nombres | |||
|---|---|---|---|
|
Nombre IUPAC
Dicloruro de disulfuro
|
|||
|
Nombre IUPAC sistemático
Diclorodisulfano |
|||
| Otros nombres
Bis [cloridosulfuro] ( S - S )
Cloruro sulfénico dimérico |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChemSpider | |||
| Tarjeta de información ECHA |
100.030.021 |
||
| Número CE | |||
| Malla | Azufre + monocloruro | ||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| un numero | 3390 | ||
|
Tablero CompTox ( EPA )
|
|||
|
|||
|
|||
| Propiedades | |||
| S 2 Cl 2 | |||
| Masa molar | 135,04 g / mol | ||
| Apariencia | Líquido aceitoso de ámbar claro a rojo amarillento | ||
| Olor | picante, nauseabundo, irritante | ||
| Densidad | 1,688 g / cm 3 | ||
| Punto de fusion | −80 ° C (−112 ° F; 193 K) | ||
| Punto de ebullición | 137,1 ° C (278,8 ° F; 410,2 K) | ||
| se descompone, con pérdida de HCl | |||
| Solubilidad | soluble en etanol , benceno , éter , cloroformo , CCl 4 | ||
| Presión de vapor | 7 mmHg (20 ° C) | ||
| −62,2 · 10 −6 cm 3 / mol | |||
|
Índice de refracción ( n D )
|
1,658 | ||
| Estructura | |||
| C 2 , torpe | |||
| 1,60 D | |||
| Peligros | |||
| Ficha de datos de seguridad | ICSC 0958 | ||
| Tóxico ( T ) Nocivo ( Xn ) Corrosivo ( C ) Peligroso para el medio ambiente ( N ) |
|||
| Frases R (desactualizadas) | R14 , R20 , R25 , R29 , R35 , R50 | ||
| Frases S (desactualizadas) | (S1 / 2) , S26 , S36 / 37/39 , S45 , S61 | ||
| NFPA 704 (diamante de fuego) | |||
| punto de inflamabilidad | 118,5 ° C (245,3 ° F; 391,6 K) | ||
| 234 ° C (453 ° F; 507 K) | |||
| Dosis o concentración letal (LD, LC): | |||
|
LC Lo ( menor publicado )
|
150 ppm (ratón, 1 min) | ||
| NIOSH (límites de exposición a la salud de EE. UU.): | |||
|
PEL (permitido)
|
TWA 1 ppm (6 mg / m 3 ) | ||
|
REL (recomendado)
|
C 1 ppm (6 mg / m 3 ) | ||
|
IDLH (peligro inmediato)
|
5 ppm | ||
| Compuestos relacionados | |||
|
Cloruros de azufre relacionados
|
Dicloruro de azufre Cloruro de tionilo Cloruro de sulfurilo |
||
|
Compuestos relacionados
|
Difluoruro de disulfuro Dibromuro de disulfuro |
||
|
Salvo que se indique lo contrario, los datos se proporcionan para materiales en su estado estándar (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referencias de Infobox | |||
El dicloruro de disulfuro es el compuesto inorgánico de azufre y cloro con la fórmula S 2 Cl 2 .
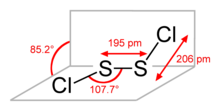
Algunos nombres alternativos para este compuesto son monocloruro de azufre (el nombre implicado por su fórmula empírica , SCl), dicloruro de disulfuro (ortografía en inglés británico) y monocloruro de azufre (ortografía en inglés británico). S 2 Cl 2 tiene la estructura implícita en la fórmula Cl − S − S − Cl, donde el ángulo entre los planos Cl a −S − S y S − S − Cl b es de 90 °. Esta estructura se denomina torpe y es similar a la del H 2 O 2 . Un isómero raro de S 2 Cl 2 es S = SCl 2 ; este isómero se forma transitoriamente cuando S 2 Cl 2 se expone a radiación UV (ver tiosulfóxidos ).
Síntesis, propiedades básicas, reacciones.
El dicloruro de disulfuro puro es un líquido amarillo que "humea" en el aire húmedo debido a la reacción con el agua. Una ecuación idealizada (pero complicada) es:
- 16 S 2 Cl 2 + 16 H 2 O → 8 SO 2 + 32 HCl + 3 S 8
Se produce por cloración parcial de azufre elemental. La reacción transcurre a velocidades utilizables a temperatura ambiente. En el laboratorio, el cloro gaseoso se introduce en un matraz que contiene azufre elemental. A medida que se forma el dicloruro de disulfuro, el contenido se convierte en un líquido amarillo dorado:
- S 8 + 4 Cl 2 → 4 S 2 Cl 2 , ΔH = −58.2 kJ / mol
El exceso de cloro produce dicloruro de azufre , lo que hace que el líquido se vuelva menos amarillo y más rojo anaranjado:
- S 2 Cl 2 + Cl 2 ↔ 2 SCl 2 , ΔH = −40,6 kJ / mol
La reacción es reversible y, al reposar, SCl 2 libera cloro para volver al dicloruro de disulfuro. El dicloruro de disulfuro tiene la capacidad de disolver grandes cantidades de azufre, lo que refleja en parte la formación de polisulfanos :
- S 2 Cl 2 + n S → S 2 + n Cl 2
El dicloruro de disulfuro se puede purificar mediante destilación del exceso de azufre elemental.
El S 2 Cl 2 también surge de la cloración de CS 2 como en la síntesis de tiofosgeno .
Reacciones
El S 2 Cl 2 se hidroliza en dióxido de azufre y azufre elemental. Cuando se tratan con sulfuro de hidrógeno, los polisulfanos se forman como se indica en la siguiente fórmula idealizada:
- 2 H 2 S + S 2 Cl 2 → H 2 S 4 + 2 HCl
Reacciona con el amoníaco para dar imida de heptasulfuro (S 7 NH) y anillos S − N relacionados S 8 − x (NH) x (x = 2, 3).
Aplicaciones
Se ha utilizado S 2 Cl 2 para introducir enlaces C − S. En presencia de cloruro de aluminio (AlCl 3 ), S 2 Cl 2 reacciona con benceno para dar sulfuro de difenilo:
- S 2 Cl 2 + 2 C 6 H 6 → (C 6 H 5 ) 2 S + 2 HCl + 1/8 S 8
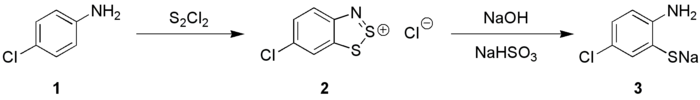
Las anilinas (1) reaccionan con S 2 Cl 2 en presencia de NaOH para dar sales de 1,2,3-benzoditiazolio (2) ( reacción de Herz ) que pueden transformarse en orto -aminotiofenolatos (3), estas especies son precursoras del tioíndigo tintes.
También se utiliza para preparar mostaza azufrada , comúnmente conocida como "gas mostaza", mediante reacción con etileno a 60 ° C (proceso Levinstein):
- S 2 Cl 2 + 2 C 2 H 4 → (ClC 2 H 4 ) 2 S + 1/8 S 8
Otros usos del S 2 Cl 2 incluyen la fabricación de tintes de azufre, insecticidas y cauchos sintéticos. También se utiliza en la vulcanización en frío de cauchos, como catalizador de polimerización de aceites vegetales y para el endurecimiento de maderas blandas.
Seguridad y regulación
Esta sustancia está incluida en la Lista 3 Parte B - Precursores químicos de la Convención de Armas Químicas (CWC). Las instalaciones que producen y / o procesan y / o consumen sustancias químicas programadas pueden estar sujetas a controles, mecanismos de notificación e inspección por parte de la OPAQ (Organización para la Prohibición de las Armas Químicas).