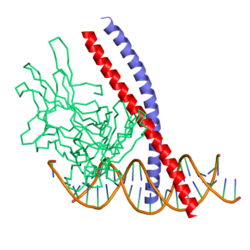
c-Fos - c-Fos
En los campos de la biología molecular y la genética , c-Fos es un protooncogén que es el homólogo humano del oncogén retroviral v-fos. Se descubrió por primera vez en fibroblastos de rata como el gen transformador del FBJ MSV (virus del sarcoma osteogénico murino Finkel-Biskis-Jinkins) (Curran y Tech, 1982). Es parte de una familia de factores de transcripción Fos más grande que incluye c-Fos, FosB , Fra-1 y Fra-2 . Se ha mapeado en la región del cromosoma 14q21 → q31. c-Fos codifica una proteína de 62 kDa, que forma heterodímero con c-jun (parte de la familia Jun de factores de transcripción), lo que da como resultado la formación del complejo AP-1 (proteína activadora-1) que se une al ADN en sitios específicos de AP-1 en las regiones promotoras y potenciadoras de los genes diana y convierte las señales extracelulares en cambios de expresión génica. Desempeña un papel importante en muchas funciones celulares y se ha descubierto que se sobreexpresa en una variedad de cánceres.
Estructura y función
c-Fos es una proteína de 380 aminoácidos con una región de cremallera de leucina básica para la dimerización y unión al ADN y un dominio de transactivación en el extremo C-terminal y, como las proteínas Jun, puede formar homodímeros. Los estudios in vitro han demostrado que los heterodímeros Jun-Fos son más estables y tienen una actividad de unión al ADN más fuerte que los homodímeros Jun-Jun.
Una variedad de estímulos, que incluyen suero , factores de crecimiento , promotores de tumores, citocinas y radiación UV, inducen su expresión. El ARNm y la proteína de c-fos se encuentran generalmente entre los primeros en expresarse y, por lo tanto, se denominan genes tempranos inmediatos . Se induce rápida y transitoriamente, dentro de los 15 minutos posteriores a la estimulación. Su actividad también está regulada por la modificación postraduccional provocada por la fosforilación por diferentes quinasas, como MAPK , CDC2, PKA o PKC que influyen en la estabilidad de las proteínas, la actividad de unión al ADN y el potencial trans-activador de los factores de transcripción. Puede provocar tanto la represión génica como la activación génica, aunque se cree que en ambos procesos intervienen dominios diferentes.
Está involucrado en importantes eventos celulares, incluida la proliferación, diferenciación y supervivencia celular; genes asociados con la hipoxia ; y angiogénesis ; lo que hace que su desregulación sea un factor importante para el desarrollo del cáncer. También puede inducir una pérdida de polaridad celular y una transición epitelio-mesenquimatosa , lo que conduce a un crecimiento invasivo y metastásico en las células epiteliales mamarias.
La importancia de c-fos en el contexto biológico se ha determinado eliminando la función endógena mediante el uso de ARNm antisentido, anticuerpos anti-c-fos, una ribozima que escinde el ARNm de c-fos o un mutante negativo dominante de c-fos. Los ratones transgénicos así generados son viables, lo que demuestra que existen vías de proliferación celular dependientes e independientes de c-fos, pero muestran una variedad de defectos de desarrollo específicos de tejido, que incluyen osteoporosis , gametogénesis retardada , linfopenia y anomalías del comportamiento.
Significación clínica
|
|
El complejo AP-1 se ha implicado en la transformación y progresión del cáncer . En el osteosarcoma y el carcinoma de endometrio, la sobreexpresión de c-Fos se asoció con lesiones de alto grado y mal pronóstico. Además, en una comparación entre la lesión precancerosa del cuello uterino y el cáncer de cuello uterino invasivo, la expresión de c-Fos fue significativamente menor en las lesiones precancerosas. c-Fos también se ha identificado como predictor independiente de disminución de la supervivencia en el cáncer de mama .
Se encontró que la sobreexpresión de c-fos del promotor del MHC de clase I en ratones transgénicos conduce a la formación de osteosarcomas debido al aumento de la proliferación de osteoblastos, mientras que la expresión ectópica de las otras proteínas Jun y Fos no induce tumores malignos. La activación del transgén c-Fos en ratones da como resultado la sobreexpresión de ciclina D1, A y E en osteoblastos y condrocitos, tanto in vitro como in vivo , lo que podría contribuir al crecimiento descontrolado que conduce al tumor. Los osteosarcomas humanos analizados para la expresión de c-fos han dado resultados positivos en más de la mitad de los casos y la expresión de c-fos se ha asociado con una mayor frecuencia de recaídas y una mala respuesta a la quimioterapia.
Varios estudios han planteado la idea de que c-Fos también puede tener actividad supresora de tumores, que podría promover y suprimir la tumorigénesis. Apoyando esto está la observación de que en los carcinomas de ovario, la pérdida de expresión de c-Fos se correlaciona con la progresión de la enfermedad. Esta doble acción podría estar habilitada por la composición diferencial de proteínas de las células tumorales y su entorno, por ejemplo, socios de dimerización, coactivadores y arquitectura promotora. Es posible que la actividad supresora de tumores se deba a una función proapoptótica. El mecanismo exacto por el cual c-Fos contribuye a la apoptosis no se comprende claramente, pero las observaciones en células de carcinoma hepatocelular humano indican que c-Fos es un mediador de la muerte celular inducida por c-myc y podría inducir apoptosis a través de la vía de la cinasa p38 MAP. El ligando Fas (FASLG o FasL) y el ligando inductor de apoptosis relacionado con el factor de necrosis tumoral (TNFSF10 o TRAIL) podrían reflejar un mecanismo apoptótico adicional inducido por c-Fos, como se observa en una línea celular de leucemia de células T humanas. Otro posible mecanismo de participación de c-Fos en la supresión tumoral podría ser la regulación directa de BRCA1, un factor bien establecido en el cáncer de mama y ovario familiar.
Además, el papel de c-fos y otras proteínas de la familia Fos también se ha estudiado en carcinoma de endometrio, cáncer de cuello uterino, mesoteliomas, cáncer colorrectal, cáncer de pulmón, melanomas, carcinomas de tiroides, cáncer de esófago, carcinomas hepatocelulares, etc.
Se ha demostrado que la cocaína, la metanfetamina, la morfina y otras drogas psicoactivas aumentan la producción de c-Fos en la vía mesocortical (corteza prefrontal) así como en la vía de recompensa mesolímbica (núcleo accumbens), además de mostrar variabilidad dependiendo de la sensibilización previa. c-Fos represión por ΔFosB 's AP-1 complejo dentro de los de tipo D1 neuronas espinosas medio del núcleo accumbens actúa como un interruptor molecular que permite la inducción crónica de ΔFosB, permitiendo así que se acumule más rápidamente. Como tal, el promotor de c-Fos se utiliza en la investigación de la adicción a las drogas en general, así como en la recaída inducida por el contexto en la búsqueda de drogas y otros cambios de comportamiento asociados con el consumo crónico de drogas.
Se ha observado un aumento en la producción de c-Fos en las neuronas que contienen receptores de andrógenos en ratas después del apareamiento.
Aplicaciones
La expresión de c-fos es un marcador indirecto de la actividad neuronal porque c-fos a menudo se expresa cuando las neuronas disparan potenciales de acción. La regulación al alza del ARNm de c-fos en una neurona indica actividad reciente.
El promotor c-fos también se ha utilizado para la investigación del uso indebido de drogas. Los científicos utilizan este promotor para activar transgenes en ratas, lo que les permite manipular conjuntos neuronales específicos para evaluar su papel en los recuerdos y el comportamiento relacionados con las drogas. Este control neuronal se puede replicar con optogenética o DREADD
Interacciones
Se ha demostrado que c-Fos interactúa con:
- BCL3 ,
- COBRA1 ,
- CSNK2A1 ,
- CSNK2A2 ,
- DDIT3 ,
- JUN
- NCOA1 ;,
- NCOR2 ,
- RELA ,
- RUNX1 ,
- RUNX2 ,
- SMAD3 y
- TBP .

|

Ver también
Referencias
Otras lecturas
- Murphy LC, Alkhalaf M, Dotzlaw H, Coutts A, Haddad-Alkhalaf B (junio de 1994). "Regulación de la expresión génica en células de cáncer de mama humano T-47D por progestinas y antiprogestinas". Tararear. Reprod . 9 Supl. 1: 174–80. doi : 10.1093 / humrep / 9.suppl_1.174 . PMID 7962462 .
- Pompeiano M, Cirelli C, Arrighi P, Tononi G (1995). "Expresión de c-Fos durante la vigilia y el sueño". Neurophysiol Clin . 25 (6): 329–41. doi : 10.1016 / 0987-7053 (96) 84906-9 . PMID 8904195 . S2CID 23760149 .
- Herrera DG, Robertson HA (octubre de 1996). "Activación de c-fos en el cerebro". Prog. Neurobiol . 50 (2-3): 83-107. doi : 10.1016 / S0301-0082 (96) 00021-4 . PMID 8971979 . S2CID 31105978 .
- Velázquez Torres A, Gariglio Vidal P (2002). "[Posible papel del factor de transcripción AP1 en la regulación específica de tejido del virus del papiloma humano]". Rev. Invest. Clin. (en español). 54 (3): 231–42. PMID 12183893 .
enlaces externos
- c-fos + Proteins en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- c-fos + Genes en los encabezados de temas médicos (MeSH) de la Biblioteca Nacional de Medicina de EE. UU .
- FactorBook c-Fos
- Kayak Drosophila - La mosca interactiva
- Ubicación del genoma humano FOS y página de detalles del gen FOS en UCSC Genome Browser .
- Descripción general de toda la información estructural disponible en el PDB para UniProt : P01100 ( protooncogén humano c-Fos) en PDBe-KB .
- Descripción general de toda la información estructural disponible en el PDB para UniProt : P01101 (Mouse Proto-oncogene c-Fos) en PDBe-KB .