Péptido beta - Beta-peptide
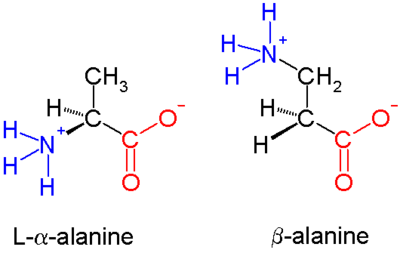
Los β-péptidos son péptidos derivados de β-aminoácidos. Los β-aminoácidos parentales son H 2 NCH 2 CH 2 CO 2 H pero la mayoría de los ejemplos presentan sustituyentes en lugar de uno o más enlaces CH. El único aminoácido β común de origen natural es la β-alanina . Los péptidos β en general no aparecen en la naturaleza. Se están explorando antibióticos basados en péptidos β como formas de evadir la resistencia a los antibióticos . Los primeros estudios en este campo fueron publicados en 1996 por el grupo de Dieter Seebach y el de Samuel Gellman.
Síntesis
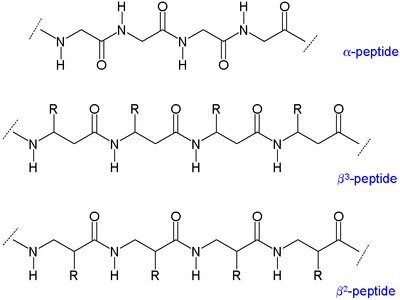
Existen dos tipos principales de péptidos β: los que tienen el residuo orgánico (R) junto a la amina se denominan péptidos β 3 y los que tienen una posición próxima al grupo carbonilo se denominan péptidos β 2 .
Los β-aminoácidos se han preparado por muchas vías, incluidas algunas basadas en la síntesis de Arndt-Eistert .
Estructura secundaria
Debido a que sus cadenas principales son más largas que las de los péptidos normales , los péptidos β forman estructuras secundarias dispares . Los sustituyentes alquilo en las posiciones α y β en un aminoácido β favorecen una conformación torpe alrededor del enlace entre el carbono α y el carbono β. Esto también afecta la estabilidad termodinámica de la estructura.
Se han informado muchos tipos de estructuras de hélice que consisten en péptidos β. Estos tipos de conformación se distinguen por el número de átomos en el anillo con enlaces de hidrógeno que se forma en solución; Se ha informado de 8 hélices, 10 hélices, 12 hélices, 14 hélices y 10/12 hélices. En términos generales, los péptidos β forman una hélice más estable que los péptidos α.
Potencial clínico
Los péptidos β son estables frente a la degradación proteolítica in vitro e in vivo , una ventaja potencial sobre los péptidos naturales. Se han utilizado β-péptidos para imitar antibióticos basados en péptidos naturales como las magaininas , que son muy potentes pero difíciles de usar como fármacos porque son degradados por enzimas proteolíticas.
Lista
Existen 8 formas beta: alanina, leucina, lisina, arginina, glutamato, glutamina, fenilalanina, formas de tirosina. El ácido aspártico se considera tanto en forma beta como alfa, aunque la forma beta se encuentra en microcistinas .