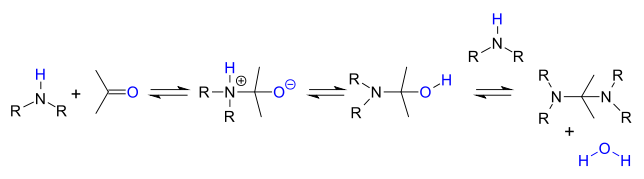Alquilimino-de-oxo-bisustitución - Alkylimino-de-oxo-bisubstitution
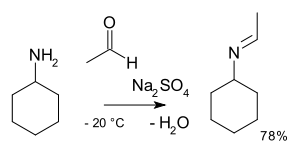
La alquilimino-de-oxo-bisustitución en química orgánica es la reacción orgánica de compuestos carbonílicos con aminas a iminas . El nombre de la reacción se basa en la nomenclatura de transformaciones de la IUPAC . La reacción es catalizada por ácido y el tipo de reacción es la adición nucleófila de la amina al compuesto de carbonilo seguida de la transferencia de un protón del nitrógeno al oxígeno a un hemiaminal estable o carbinolamina. Con las aminas primarias, el agua se pierde en una reacción de eliminación de una imina . Con arilo aminas especialmente estables bases de Schiff se forman.
Mecanismo de reacción
Las etapas de reacción son reacciones reversibles y la reacción se completa mediante la eliminación de agua, por ejemplo, mediante destilación azeotrópica , tamices moleculares o tetracloruro de titanio . Las aminas primarias reaccionan a través de un intermedio hemiaminal inestable que luego se separa del agua.
Las aminas secundarias no pierden agua fácilmente porque no tienen un protón disponible y, en cambio, a menudo reaccionan más a un aminal :
o cuando un protón de α-carbonilo está presente en una enamina :
En ambiente ácido, el producto de reacción es una sal de iminio por pérdida de agua.
Este tipo de reacción se encuentra en muchas preparaciones de heterociclo, por ejemplo, la reacción de Povarov y la síntesis de Friedländer a quinolinas .
Debido a que ambos componentes son tan reactivos, una molécula no lleva un aldehído y un grupo amina al mismo tiempo, a menos que el grupo amina esté equipado con un grupo protector . Como demostración adicional de reactividad, un estudio exploró las propiedades de una α- formil aziridina que se encontró que se dimerizaba como una oxazolidina al formarse a partir del éster correspondiente por reducción orgánica con DIBAL :
La formación de iones imonio está prohibida en esta molécula porque se dice que el grupo aziridina y el grupo formilo son ortogonales .
Alcance
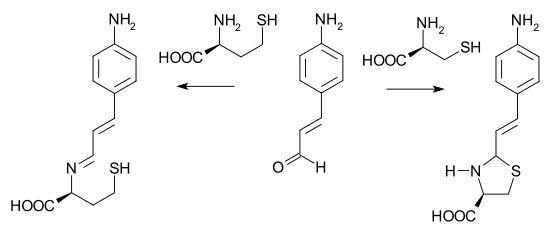
En una aplicación potencial, p -amino cinamaldehído es capaz de diferenciar entre la cisteína y la homocisteína . Con la cisteína, una solución acuosa tamponada del aldehído cambia de amarillo a incoloro debido a una reacción secundaria de cierre del anillo de la imina. La homocisteína es incapaz de cerrar el anillo y el color no cambia.
Referencias
enlaces externos
- reacción de benzaldehído y metilamina en Organic Syntheses Coll. Vol. 10, pág. 312 (2004); Vol. 76, pág. 23 (1999). Articulo en linea
- reacción de metilbencilamina con 2-metilciclohexanona en Organic Syntheses , Coll. Vol. 9, pág. 610 (1998); Vol. 70, pág. 35 (1992). Artículo
- Reacción de acetofenona con metilamina en síntesis orgánica , Coll. Vol. 6, pág. 818 (1988); Vol. 54, pág. 93 (1974). Artículo
- Base Chiral Schiff en Molbank 2005, M435 Artículo